|
■微生物検査 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■細菌培養検査の注意点 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
1)
血液培養陽性結果の連絡体制について 平日日勤帯:病棟または主治医に電話連絡+塗抹グラム染色結果を含めて検査結果画面を更新 夜間帯と土日祝日:病棟に電話連絡+カルテ記載(MID webで塗抹標本の顕微鏡画像が確認可能) 口頭ではグラム染色結果が間違って伝達される場合があるので、必ず検査結果画面で確認すること。 2)
血液培養採取について コンタミネーションの区別のために、可能な限り2セット(4本)、2箇所から採取することが望ましい。手指消毒の上、手袋をつけて行うこと。中心静脈カテーテル感染が疑われるときは、末梢とカテーテルからそれぞれ採取する。 3)
監視培養検査について 伝播防止または手術時の感染予防等を目的とした耐性菌保菌者のスクリーニング検査を実施する。 MRSAは鼻腔拭いをスワブで採取し、耐性菌の発育のみを確認する。オーダーは『MRSA監視培養タブ』を選択する。ICU・救急監視培養は、カルバペネム耐性またはカルバペネマーゼ産生腸内細菌目細菌、耐性緑膿菌(カルバペネム系薬単剤耐性、カルバペネム系薬・キノロン系薬・アミノグリコシド系薬のうち2剤または3剤耐性)、耐性Acinetobacter baumannii complex(カルバペネム系薬・キノロン系薬・アミノグリコシド系薬いずれかに耐性)を対象とする。前述の対象菌は選択培地を用い発育菌の感受性検査を実施するが、それ以外の発育菌は同定検査のみ行うとする。オーダーは『ICU監視培養タブ』または『救急監視培養タブ』を選択する。費用は病院負担とし、保険請求はしない。 詳細なオーダー方法については「接触予防策・監視培養」内の「監視培養検査」を参照する。 4)
不必要・不適切な検体提出を控える 保険適応となる検体数は、呼吸器系、皮膚創部、便等それぞれ1検体だけである。不必要な数の検体は、経費と労力を要するため控えること。膿汁は可能な限り無菌的に採取、また喀痰はうがいをして膿性のものを提出すること。 5)
時間外の検体の保存 検体は土日および時間外でも基本的に検査部緊急検査室で預かる。止むを得ず病棟で保存する場合は冷蔵保存する。ただし、髄液や眼脂などの増菌培地および血液培養は時間外も含め採取後直ちに検査部に提出する。 6)
検査オーダーの注意点 迅速かつ的確に菌を検出するためには、選択培地という特定の菌種のみを発育させる培地を使用するため「目的菌」を入力する。特にMRSA、緑膿菌などの耐性菌が疑われる場合や便培養は目的菌を明確にする必要がある。 7)
便培養検査 目的菌を選択しオーダーする。入院72時間以降で抗菌薬関連下痢症が疑われる場合は、基本的にCDトキシン迅速検査を依頼する。治療したCDI患者の隔離解除の判断を目的とした迅速検査は行わない。また多剤耐性緑膿菌などの薬剤耐性菌の監視培養を行うときは、上記「3)監視培養検査について」を参照。 8)
嫌気培養検査 嫌気培養検査は、以下の重要度(表1)や因子(表2)を評価して検査を行うことを推奨する。評価後、嫌気性菌感染症を積極的に疑う場合のみ、嫌気培養検査をオーダーすることを遵守する。その場合、検体は嫌気ポーターを使用して提出することを遵守する。また、時間外に検体を提出する場合は、嫌気状態を保持するため、嫌気ポーターを使用して提出する。嫌気ポーターは、細菌検査室に取りに行く(時間外は時間外検査室へ取りに行く)。また、オーダーはないが、下表1のA-1〜A-3、Bの1〜6の場合に嫌気性菌の菌量が多い場合、検査技師より診療科へ嫌気培養検査の追加のオーダー(嫌気培養同定)を依頼することがある。 表1 嫌気性菌検査を行う臨床材料の重要度分類
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
臨床微生物検査ハンドブック第5版
より引用・改変 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
表2 嫌気性菌感染症を疑う因子 1.
悪臭あり 2.
閉鎖性の腫瘍(脳腫瘍、肺腫瘍、成人の膿胸、歯周部の膿、皮下腫瘍など) 3.
腹腔内感染症(肝腫瘍、横隔膜下腫瘍など) 4.
婦人性器感染症(膣炎、付属器炎など) 5.
塗沫検査陽性、好気培養陰性の材料 6.
アミノグリコシド系が無効な感染症 7.
抗菌薬投与後の下痢症(C. difficile 偽膜性大腸炎) 8.
ABPCやCEZが無効な感染症(B. fragilisなど) 9.
壊疽、土で汚染された壊死組織(Clostoridioidesなど) 10.
膿汁中のドルーゼ(硫黄顆粒、菌塊)ーActinomyces 臨床微生物検査ハンドブック第5版
より引用・改変 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■検体の採取法 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
1)
喀痰:口腔内常在菌の混入を防ぐ、水でうがいや歯磨きをしたのち容器に喀出してもらう。イソジンや抗菌薬入りの歯磨き粉は使わない。喀痰の性状(色、膿性、唾液成分など)は医師が自ら確認すべきである。 2)
採尿:カテーテル尿、中間尿を提出する。尿路感染症を疑わせる混濁尿かどうかを確認し、また尿沈渣で白血球数を調べる。 3)
皮膚:常在菌の混入を防ぐため、膿性部分を採取する。水疱では、表面を消毒したのちに穿刺する。嫌気培養が必要な場合は、可能な限り短時間で採取し、嫌気ポーターに入れて提出する。 |
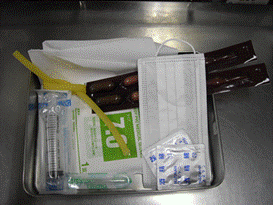
喀痰・便容器、滅菌スピッツ、嫌気ポーター、スワブ |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■検体の輸送と管理 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
【検体の搬送方法】 検体は、ビニール袋またはプラスチック製の搬送容器に入れ細菌検査室へ搬送する。なお、搬送容器は、各部署で管理する。メッセンジャー搬送の場合は、プラスチック製の容器に入れた状態で、各部署から搬送する。 1)
検体は、原則としてすぐに細菌検査室に運搬する。土日および時間外でも検査部緊急検査室で預かり可能である。 2)
検体をすぐに運べない場合は、冷蔵保存(喀痰、尿など)する。淋菌や髄膜炎菌は低温に弱いため、疑われる場合は冷蔵保存しない。髄液は決して冷蔵保存しないこと。 3)
細菌は乾燥で死滅しやすいので、チューブには少量の滅菌生理食塩水を一緒に入れる。綿棒採取では特に注意する。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■検体の性状(喀出痰) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
肉眼による評価
|
鏡検による評価
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
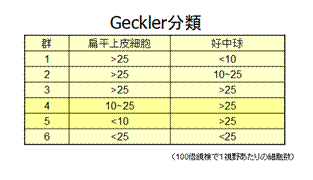
1) 微生物検査に適した膿性部分を多く含む良質痰を提出する 2) 喀出痰の肉眼的評価は法としてMiller & Jones分類を使用する 原因菌の判定にはMiller
& Jones分類はP2以上、Geckler分類は4~5群が望ましい。THINK画面で検体の上記品質評価を確認できるので、適正な喀痰検体であったかを確認すること。 3) Miller
& Jones分類M1の喀出痰が提出された場合は、細菌検査室では受け取らず採り直しを依頼する(抗酸菌検査は対象外とする)。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■検体の性状(便) ※C.difficile感染症(CDI) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
(ア)
微生物検査には、有形便では拇指頭大、水様便では容器の1/5程度提出する (イ)
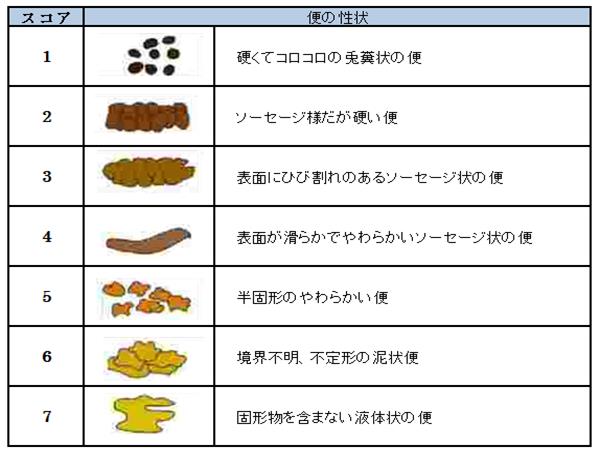
便の性状は、ブリストル便形状スケールを用いる(表2) (ウ)
CDIを疑った際には、ブリストル便形状スケールのスコア5以上の便を検査に提出する (エ)
ブリストル便形状スケールのスコア1〜4の便が提出された場合は、細菌検査室では受け取らず採り直 しを依頼する。
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■検体の性状(便) ※C.difficile感染症(CDI) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
1)
血液培養の採取は原因菌を正確に同定するためにきわめて重要である。 2)
菌血症を疑う患者すべてが対象となる。肺炎、骨髄炎、意識障害やショックの患者も対象となる。 3)
採血を抗菌薬投与前に行う。すでに抗菌薬が投与されている場合は次回投与直前に採血する。 4)
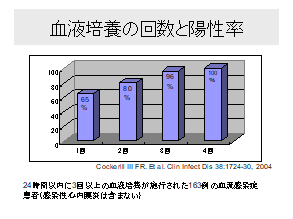
少なくとも2セット(4本)、2箇所から。コンタミネーションの区別が可能になり、また検出率が上昇する。カテーテル感染を疑う場合は、末梢とカテーテルから採取。 5)
1回目の後すぐに2セット目の採血をしても構わない。 静脈血と動脈血で陽性率に差はないため、採血は静脈血で可。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
小児で必要な採血量 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kellogg et al. JCM 2000; 38:
2181-5より一部改変 1) CVカテーテルだけからの血液採取は菌が検出されたとしても血流感染を起こしているかの判断が難しいため、原則として行わない。 培養ボトルの注射針穿刺部位は必ずしも無菌ではないため、アルコールで消毒する。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■検査結果の見方 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
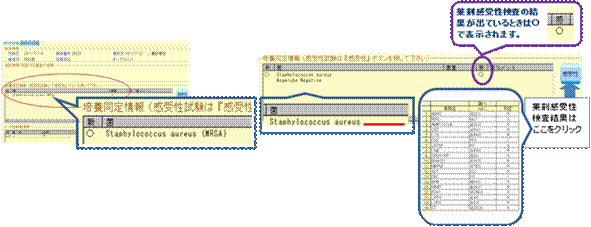
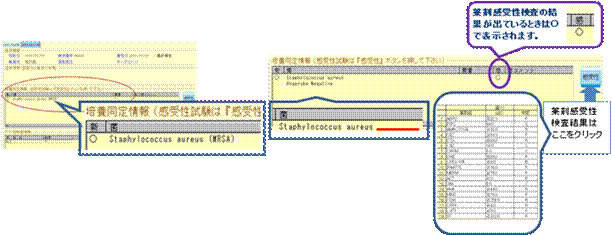
1) MRSA (メチシリン耐性黄色ブドウ球菌) 培養同定情報に表示される。MSSA(メチシリン感受性黄色ブドウ球菌)は薬剤感受性結果の後判定され、特に表示されない。またMRSはメチシリン耐性コアグラーゼ陰性ブドウ球菌のことであり、接触感染予防策ではなく標準予防策で対応可能である。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
2) ESBL(基質拡張型βラクタマーゼ産生菌)、多剤耐性菌 菌コメント、報告コメント情報に表示される。薬剤感受性検査の確認も必要である。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■グラム染色の解釈基準 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■培地の菌量表現 (定量・半定量) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■一般細菌薬剤感受性検査 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
1)
薬剤感受性検査の実施条件 1)無菌的な材料(血液培養ボトル・髄液・穿刺液など)から菌が検出された場合 菌量の幾分にかかわらず感受性検査を行う。但し、実施頻度は、初回検出時と前回検出時から7日以上を経過して検出された場合のみとする。また、対象菌が起炎菌として推定されないコンタミネーションを疑う菌(常在菌等)の場合は、主治医と相談の元、感受性検査は行わないとする。 *血液培養ボトル、髄液、穿刺液を除く、術中の採取検体や閉鎖的部位から採取した検体などを無菌的な材料として提出する場合は、検査オーダーへ「無菌的な材料」を示すコメントを記載する。記載のない検体は、無菌的な材料としてみなさない。 2)検体(無菌的な材料を除く)から菌が検出された場合 菌量が少数の場合や、対象菌が常在菌(口腔内常在菌、皮膚常在菌、尿道常在菌、膣内常在菌 など)の場合は、菌量の幾分にかかわらず感受性検査は行わないとする。前述以外の起炎菌が菌量 1+以上検出された場合は、初回検出時と前回検出時から7日以上を経過して検出された場合のみ 感受性検査を行う。 2)
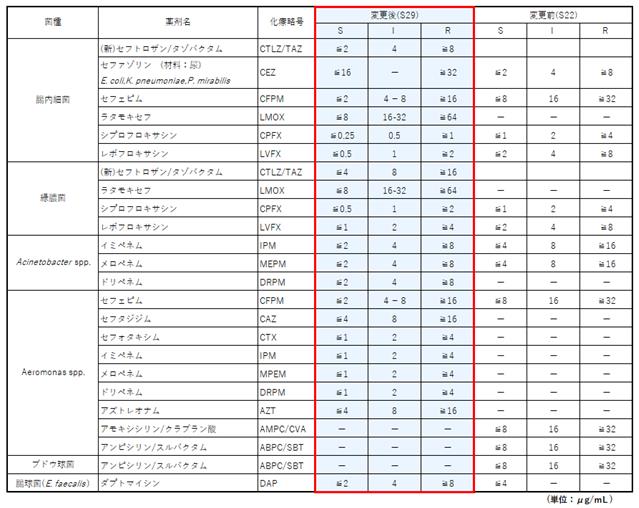
判定基準 2025年7月14日受付分よりから判定基準・ブレイクポイントをCLSI(Clinical and Laboratory Standards Institute) M100-S29からM100-S34へ変更した。 【判定基準変更薬剤一覧】 赤字:S29から変更したブレイクポイント 《グラム陰性桿菌》 【腸内細菌】 *大きな変更点:Salmonella属/Shigella属が他の腸内細菌と独立した。
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
【緑膿菌】
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
【アシネトバクター属菌】
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
【Stenotrophomonas maltophilia】
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
【ヘモフィルス菌】
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
《グラム陽性球菌》 【ブドウ球菌】
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
【腸球菌】
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
【肺炎球菌】
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■β-D-グルカン |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
クリプトコックス症、ムーコル症を除く深在性真菌症に対する血清診断法の一つである。当院で使用している測定キットは希釈加熱-比濁時間分析法(ワコー法)であり、特異度に優れている。カットオフ値は11pg/mLである。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
■新型コロナウイルスの検査(PCR, 抗原定量検査) |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||