|
B.2. �x�� |
||||||||||||||||||||||||||||||
|
1. �x���̒�` �x���́u�x�����́C�}���́C�����ǂ́C���ǁv�ƒ�`���邱�Ƃ��ł��C���Ǖp�x�C�����\��C�����̎��iQOL�j�C�Љ�ɗ^����e���Ȃǂ̓_�ōł��d�v�Ȋ����ǂ̂ЂƂł���D 2. �x���̗Տ��I���� �x���͔��ǂ̏��a�Ԃ̊ϓ_����́C�s���x���icommunity-acquired pneumonia : CAP�j�C���@48���Ԉȍ~�ɔ��ǂ���@���x���iHospital-acquired pneumonia : HAP�j�C��Â�����Ă���l�ɔ��ǂ����ÁE���֘A�x���iNursing and healthcare-associated
pneumonia : NHCAP�j�ɑ�ʂ��邱�Ƃ��ł���D��ʓI�ɁCCAP���҂͊�b������L���Ă��炸�i�܂��͗L���Ă��y���ł���j�C�ϐ��ۂ������ۂƂȂ�p�x�����Ȃ��DNHCAP�͎�Ɉ�ÃP�A������鍂��҂ɔ��ǂ���x���ł���C�J��Ԃ��뚋���x���ɑ�\�����\��s�ǂ̏I�����x���̑���悷���������DHAP�͓��@��48���Ԉȏ�o�߂��Ă���V�������ǂ����x���ƒ�`����C���@�����łɊ������Ă������̂͏������D |
||||||||||||||||||||||||||||||
|
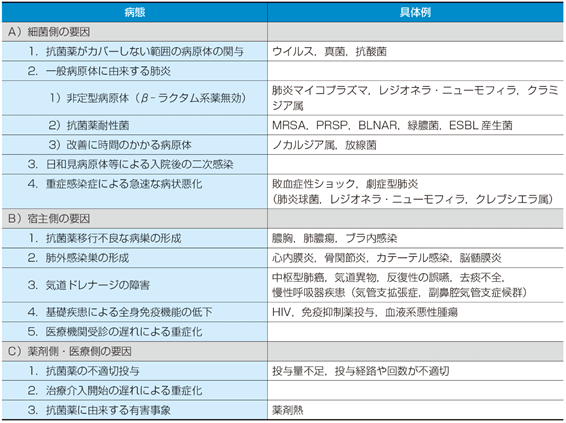
1. ��` �@�s���x���́A�a�@�O�œ��퐶�����c��ł�����b������L���Ȃ��A���邢�͗L���Ă��y���Ȋ�b�����̐l�ɋN����x���ł���B �@�s���x�����@���x�����ÁE���֘A�x���Ƒ傫���قȂ�_�́A�����������̈Ⴂ�ŁA�s���x���ł͔��^�a���́i�x���}�C�R�v���Y�}�A�N���~�W�A���A���W�I�l���E�j���[���t�B���A�R�N�V�G�����j���l������K�v������B 2. �N���ۂɂ��� �@�s���x���̋N���ۂł́A�ې��x���̋N���ۂł���x�����ہA�C���t���G���U�ہA���F�u�h�E���ہA�x�����ۂ������A���̎��ɁA���^�x���̋N���ۂł���x���N���~�W�A�A�x���}�C�R�v���Y�}���p�x�Ƃ��đ����B����ȍ~�́A�Δ^�ہA�����N�Z���E�J�^���[���X�A�咰�ہA���W�I�l���E�j���[���t�B���̏��ƂȂ��Ă���B 3. �d�Ǔx���� �@�s���ǂ̗L���̕]���ƁA�s���x���̏d�Ǔx�]����A-DROP�V�X�e���ɂ��]�������������i�\�P�j�BA-DROP�V�X�e����p���ďd�Ǔx���ނ��s���A�d�Ljȏ�͓��@���Â��]�܂����i�\�Q�j�B �\�P�@A-DROP�V�X�e�� �\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\ A�iAge�j�F�j��70�Έȏ�A����75�Έȏ� D�iDehydration�j�FBUN 21mg/dL�ȏ�܂��͒E������ R�iRespiration�j�FSpO2 90%�ȏ�iPaO2 60torr�ȉ��j O�iOrientation�j�F�ӎ��ϗe���� P�iBlood Pressure�j�F�����i���k���j90mmHg�ȉ� �\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\ �y�ǁF��L5�̍��ڂ̂�������������Ȃ����́B �����ǁF��L���ڂ�1�܂���2��L������́B �d�ǁF��L���ڂ�3��L������́B ���d�ǁF��L���ڂ�4�܂���5��L������́B �������A�V���b�N������P���ڂ݂̂ł����d�ǂƂ���B �\�Q�@�d�Ǔx���ނƎ��Â̏�̊W �\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\ �y�ǁ|�O������ �����ǁ|�O���܂��͓��@ �d�ǁ|���@���� ���d�ǁ|ICU���@ 4. �s���x���̐f�f�ƕa���̌����@ �@�s���x���̐f�f�ł́A�����o�Ǐ�Ƃ��ĊP�AႁA���M�A�ċz����A���ɂȂǂ̋Ǐ��Ǐ�┭�M�⌑�ӊ��Ȃǂ̑S�g�Ǐ�̗L�����m�F����B�������A����҂̏ꍇ�́A�����̌ċz��Ǐ���������A�H�~�ቺ�Ȃǂ̌ċz��ȊO�̏ǏO�ʂɏo��ꍇ�����邽�ߒ��ӂ��K�v�ł���B�x���̊m��f�f�́A����X������ы���CT�Ȃǂ̉摜�f�f�ɂ���čs����B�s���x���ł́A�@���x�����ÁE���֘A�x���ƈقȂ�A�ې��x�������łȂ��A���^�x�����l������K�v������B�ې��x���Ɣ��^�x���̊ӕʂ͕\�R��p���čs���A���̌��ʂ���Ɏ��Â��s���B�\�R��6���ڒ�4���ڈȏ㍇�v�����ꍇ�͔��^�x�����^���A�U���ڒ��R���ڈȉ��̍��v�ł���ې��x�����^����B �@�s���x���̕a���̂Ƃ��āA��ʍہA�x���}�C�R�v���Y�}�A�N���~�W�A���A���W�I�l���E�j���[���t�B���A�E�C���X�Ȃǂ���������B��������������肵�R�ۖ��I������K�v�����邪�A���Տ��ł́A�O�����f���Ɏs���x���̌�������������������P�[�X�͂܂�ł���A�ʏ�̓G���s���b�N�Ɏ��Â��J�n����邱�Ƃ������B�������A�G���s���b�N���Â��s���ꍇ�ł��A�ŏ��̎��Â���������Ƃ͌���Ȃ����ߌ��������������̂��߂̌�����I�m�Ɏ��{����B�a���̂̎�ނɂ���ēK�Ȍ����@���قȂ邽�߁A�Տ��Ǐ��摜�������猴����������������x���肵������I������K�v������i�\�S�j�B (1) �O�������F �@�O�������F�͐v�����ɗD��s���x���̐f�f�ɂ����ėL�p���������B�|�{���ʂ���Ƃ����ꍇ�A�\ႂ̃O�������F�̊��x�͗ǎ��Ȍ��̂�p�����ꍇ�A60〜70%���x�Ƃ���������B�\ႂ̕i���Ƃ��ẮAMiller &Jones���ނ�P2�ȏ�AGeckler���ނ�4〜5���]�܂����B (2) �|�{�E���� �@���ۂɋۂ����ē��肷�邱�ƂŌ����ۂ̐f�f���\�ƂȂ�A��܊����������{���邱�ƂŁA�e��܂ւ̊���]�����ϐ��̗L�����m�F���邱�Ƃ��ł���B (3) ���t�|�{ �@���t�|�{�͐^�̌����ۂ̌���ɗL�p�Ȍ����ł��邪�A���o���͒Ⴍ�A�z������10%���x�ƍl�����Ă���B (4) �R�����o �@�s���x����ΏۂƂ����R�����o�́A�x�����ہA���W�I�l���E�j���[���t�B���A�x���}�C�R�v���Y�}�A�q�g���^�j���[���E�C���X�A�A�f�m�E�C���X�ARS�E�C���X�A�C���t���G���U�E�C���X�Ȃǂ��\�ł���B�x�����ۂƃ��W�I�l���E�j���[���t�B����ΏۂƂ����A���R���́A�x�����nj㐔�����ɂ킽���đJ�����Č��o����邱�Ƃ�����A�x�����J��Ԃ����ǂ��Ă���Ǘ�ł́A�������ɂ��U�z���̉\��������B���W�I�l���E�j���[���t�B�������^1�ȊO�̌����^�̋ۂ͊��x���Ⴍ�A�U�A���ƂȂ�\��������B (5) ��`�q���� �@�x���}�C�R�v���Y�}��W�I�l���E�j���[���t�B����LAMP�@��p������`�q����������B (6) �����f�f �@�ʏ�A����������2�T�Ԍ�̃y�A������p���āA�R�̉���4�{�ȏ�㏸���Ă���Ηz���Ɣ��f�����B�x���N���~�W�A�����ǂ͍R�N���~�h�t�B���E�j���[���j�G�R�̂̑���ɂ��f�f�����ꍇ�������B�������҂�N���~�W�A�E�g���R�}�`�X��I�E���a�N���~�W�A�ȂǂƂ̌��������ɂ��U�z���̖�肪����B �\�R�@�s���x���ɂ�����ې��x���Ɣ��^�x���̊ӕʍ��� �\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\ �P�A�N��60�Ζ��� �Q�A��b�������Ȃ��A���邢�͌y�� �R�A��łȊP������ �S�A�������f�㏊�����R���� �T�Aႂ��Ȃ��A���邢�͐v���f�f�@�Ō����ۂ��ؖ�����Ȃ� �U�A����������������10,000/��L�����ł��� �\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\ �\�S�@�ċz�튴���ǂ̕a���̕ʂɂ݂������̓K��
5. ���� (1) �s���x���̃G���s���b�N���ÍR�ۖ� �@�s���x���̎��Âŏd�v�Ȍ����ۂ́A�p�x�������d�lj����₷���x�����ہA�����ŃC���t���G���U�ۂł���B��N�҂̏ꍇ�͔x���}�C�R�v���Y�}�̕p�x����r�I�����A�y�ǗႪ�����B�����S�����ȂNJ�b�����ۗL���҂ɂ����Ă͔x�����ہA�C���t���G���U�ۂɎ����Ń����N�Z���E�J�^���[���X���l������B����҂ł͌��o�������T���ۂ⌙�C���ۂ̊֗^���������B A) �O�����ҌQ(�y��〜�����ǔx��) �ې��x�����^����ꍇ�ɂ́A�y�j�V�����n����A���^�x�����^����ꍇ�ɂ̓}�N�����C�h�n���I������B�����̌ċz�펾��������ꍇ�̓��X�s���g���[�L�m�������1�I���Ƃ��邪�A���j�ɑ���R�ۗ͂�L���Ă���A�g�p�ɍۂ��Ă͌��j�̗L����T�d�ɔ��f����B ������ �ECVA/AMPC(�I�[�O�����`��) �o��(125mg/250mg)
1��2�� 1��3〜4��(�Y�t�����ő�4��/��) �ECVA/AMPC(�I�[�O�����`��) �o��(125mg/250mg)
1��1�� 1��3�� �{AMPC(�r�N�V����) �o��(250mg) 1��1�� 1��3�� �EAZM(�A�W�X���}�C�V��)�������܌o��1��2g�E�P�^ �ECAM�i�N�����X���}�C�V���j 1��200mg�E1��2�� ���˖� �ECTRX(�Z�t�g���A�L�\��) �_�H�Ò� 1��2g 1��1��܂���1��1g 1��2�� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �EAZM(�A�W�X���}�C�V��) �_�H�Ò� 1�� 500mg 1��1�� B) ��ʕa�����@���ҌQ(������〜�d�ǔx��) �@���@���K�v�Ȋ��҂ɑ��Ă͏����ɐÒ���ŊJ�n���A�\�Ȃ�Α����ɓ�����փX�C�b�`����B ���˖� �ESBT/ABPC(���i�V���E�X���o�V����) �_�H�Ò� 1��3g 1��3〜4�� �ECTX(�N���t�H����) �_�H�Ò� 1��1〜2g 1��2〜3��(�Y�t�����ő�4g/��) �ECTRX(�Z�t�g���A�L�\��) �_�H�Ò� 1��2g 1��1��܂���1��1g 1��2�� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �� ���^�x�����^����ꍇ �EMINO(�~�m�T�C�N����) �_�H�Ò� 1��100mg 1��2�� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �EAZM(�A�W�X���}�C�V��) �_�H�Ò� 1�� 500mg 1��1�� C) �W�����Î��������ҌQ(�d��〜���d�ǔx��) �@�W�����Î��őS�g�Ǘ����K�v�ƂȂ�d�ǔx���̑�\�I�Ȍ��lj������ۂ͔x�����ۂƃ��W�I�l���E�j���[���t�B���ŁA���̂ق��Δ^�ۂ��܂ރO�����A�����ہA���F�u�h�E���ہA�I�E���a�N���~�W�A�A�C���t���G���U�E�C���X�Ȃǂ�����B ���˖� A�@�F �ETAZ/PIPC(�^�]�s�y) �_�H�Ò� 1��4.5g 1��3〜4�� �EIPM/CS(�`�G�i��) �_�H�Ò� 1�� 0.5〜1g 1��2〜4��(�Y�t�����ő�2g/��) �EMEPM(�����y�l��) �_�H�Ò� 1��1g 1��2〜3�� �EBIPM(�I���K�V��) �_�H�Ò� 1�� 0.3〜0.6g 1��3〜4��(�Y�t�����ő�1.2g/��) �EDRPM(�t�B�j�o�b�N�X) �_�H�Ò� 1�� 0.5〜1g 1��3�� B�@�F ���Δ^�ۂ��l�����Ȃ��ꍇ �ESBT/ABPC(���i�V���E�X���o�V����) �_�H�Ò� 1��3g 1��3〜4�� �ECTX(�N���t�H����) �_�H�Ò� 1��1〜2g 1��2〜3��(�Y�t�����ő�4g/��) �ECTRX(�Z�t�g���A�L�\��) �_�H�Ò� 1��2g 1��1��܂���1��1g 1��2�� C�@�F �EA or B�@�{AZM(�A�W�X���}�C�V��) �_�H�Ò� 1�� 500mg 1��1�� D�@�F �EA or B�@�{LVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �EA or B�@�{CPFX(�V�v���L�T��) �_�H�Ò� 1�� 300mg 1��2�� �EA or B�@�{PZFX(�p�Y�N���X) �_�H�Ò� 1�� 500〜1000mg 1��2�� E�@�F �EA or B�@ or C or D�@�{VCM(�o���R�}�C�V��) �_�H�Ò� 1��1g(�܂���15mg/kg) 1��2�� �EA or B�@ or C or D�@�{TEIC(�e�C�R�v���j��) �_�H�Ò� 2����1��400mg 1��2�[�f�B���O�A3���ڈȍ~1��400mg 1��1��(�Y�t�����ő� 800mg �����A�ȍ~400mg/��) �EA or B�@ or C or D�@�{LZD(�U�C�{�b�N�X) �_�H�Ò� 1��600mg 1��2�� (2)�@�X�C�b�`�Ö@�̖ڈ� �@�Ò��R�ۖ�̓��^�ɂ��x�����҂̏�Ԃ����P���A�@�z���Ԃ����肵�A�A�Տ��Ǐ��P���A�B�o���ێ悪�\�A�C������@�\�����S�ł���A�����R�ۖ�ւ̃X�C�b�`���\�Ƃ����B�X�C�b�`�Ö@�̊�Ƃ��āA�@�ċz��Ǐ�i�P�A�ċz����A�Ȃǁj�̉��P�A�ACRP<15mg/dL�A�B�o���ێ�̏\���ȉ��P�A�C�̉������Ȃ��Ƃ�12���Ԉȏ�38�������ł��邱�ƁA��4���ڂ����Έ��S�Ɏ��{�ł���ƕ���Ă���B (3)�@���Ê��Ԃ̖ڈ� �@�s���x���̎��Ê��Ԃ́A�y�ǂ��璆���ǂŏ������Â��t�����Ă���ꍇ�ɂ͂P�T�Ԉȓ��i5〜7���ԁj���A�d�Ǘ��A���lj��E����𗈂������郌�W�I�l���E�j���[���t�B����MRSA�A�Δ^�ۂȂǂ������ۂ̏ꍇ��A�x�O�ɂ��������L�����Ă���ꍇ�ɂ�7〜14���ԁi�ȏ�j����{�ł���i�\�T�j�B �\�T�@�s���x���ɂ����鎡�Ê��Ԃ̖ڈ� �\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\�\ �E�x�����ہF�ی��ǂ��Ȃ���Ή�M��3�i〜5�j���ԁi�Œ�5���ԁj�A�ی��Ǖ����ł�10〜14���� �E�u�h�E���ۂ⌙�C���ۂɂ����x���F14���Ԉȏ� �E���W�I�l���E�j���[���t�B���F7〜14���� �E�Δ^�ہF10〜14���� �E���̑���CAP�F�Œ�5���Ԃ���2〜3���ԕ��M���������� �E�x���^�ǁA�������A�^�������Ă���ꍇ�A��b�����ɂ������F�߂�ꍇ�ɂ́A�R�ۖ����L��蒷���ԓ��^����ׂ��ł��� |
||||||||||||||||||||||||||||||
|
B.2.2 ��ÁE���֘A�x���iNursing and healthcare-associated pneumonia :
NHCAP�j |
||||||||||||||||||||||||||||||
|
��ÃP�A������Ă���l�ɔ��ǂ���x���ł���A�ȉ��̒�`���ڂ�1�ȏ㖞�����B NHCAP�̒�` 1. �×{�a���E���_�a���ɓ��@���Ă���A�������͉��{�݂ɓ������Ă��� 2. 90���ȓ��ɕa�@��މ@���� 3. ���iPS3�F����ꂽ�����̐g�̉��̂��Ƃ����ł��Ȃ��E������50���ȏ���x�b�h���֎q�ʼn߂����A��ڈ��Ƃ���j��K�v�Ƃ��鍂��ҁE�g�̏�V�� 4. �ʉ@�Ōp���I�Ɍ��Ǔ����Ái���́E�R�ۖ�E���w�Ö@�E�Ɖu�}���j���Ă���B NHCAP�ɂ��Ă�CAP�ŕW�I�ɂ���Ȃ��ϐ��ہiMRSA, �Δ^�ہj����20���ȏ�ɕ�������邪�A�@���x��(HAP)���͑����Ȃ��A�x�����ہE�w���t�B���X���EMSSA�Ȃ�CAP�ɑ����݂���ۂɉ����A���o�������T���ہE�����ہi�N���u�V�G�����Ȃǁj�⌙�C���ۂ̕p�x�������Ă��邱�Ƃ�����Ă���B �@NHCAP�͌뚋���x���ƃI�[�o�[���b�v����ƍl�����A�����ۂ̕]����ۊw�I���ʔ��肪����Ȃ��Ƃ������B�\��s�ǂ̏I�����x���̑���悷����V���̌o�߂Ŕ��ǂ����������A�K�ȍR�ۖÂ������\������P����Ƃ͌���Ȃ����Ƃɂ����ӂ��Ă����K�v������B �@NHCAP�̏d�Ǔx��A-DROP�Ŕ��肵��q�̉@���x��(HAP)�̑ϐ��ۃ��X�N��]�����AHAP�̃G���s���b�N���ÂŎ��ÍR�ۖ�f����B�{�l�E�Ƒ��̈ӎu���������Ԃ������]�ނ��Ƃɂ������Ƃ��ɂ͍R�ۖ�g�p��escalation���邢��de-escalation�헪���I�����ɏオ���Ă悢�B�J��Ԃ��뚋���x���ɂ����ADL�����X�ɒቺ���A�I�����x���̑���悷��ꍇ�ɂ͑ϐ��ۂ�z�肵�����ÑI���͕K�v�Ȃ��Ƃ�������������B����A�o�ljh�{�Ǘ��Ǘ�E�@���ŋN�����뚋���x���E�����ۉȍۂ̊֗^���l������ꍇ�͑ϐ��ۃ��X�N���l����de-escalation���Â��l������B |
||||||||||||||||||||||||||||||
|
B.2.3�@�@���x���iHospital-acquired pneumonia : HAP�j |
||||||||||||||||||||||||||||||
|
1. �@���x���̗Տ��I���� HAP�͍��x��Â̌��ʂƂ��Ă̖Ɖu�}�����̊��҂ɐ����邱�Ƃ������D�@�����ɐ�������ۂɖ\�I����邱�Ƃ����������C�R�ۖ�̊����^�����邽�߂ɕa�@�����ŔF�߂����ܑϐ��ۂɂ��x���̌`����邱�Ƃ������D�l�H�ċz��֘A�x���iventilator-associated pneumonia :
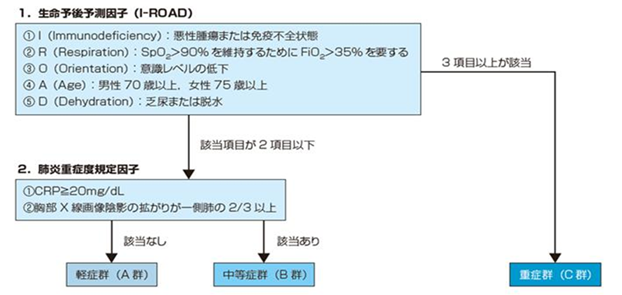
VAP�j�͋C�Ǒ}�ǁE�l�H�ċz�J�n��48���Ԉȍ~�ɐV���ɔ��ǂ����x���ł���CHAP�̒��ł����d�Ǔx�̍������ҌQ�ɐ����邱�Ƃ���C���̎��Âɂ͂Ƃ�킯��a����D���{�ɂ�����x���Q�ʂ̎��S���ɂ��ẴV�X�e�}�e�B�b�N���r���[�ɂ��C�x���̎��S���͂��ꂼ��CAP6.3%�CNHCAP15.5%�CHAP30.4%�CVAP32.4%�Ƃ̌��ʂł������D HAP���҂ɂ����錟�o�ۂ́CCAP�ƈقȂ�ϐ��ۂ������X��������D���{�ɂ�����HAP�̉u�w�����̊���ΏۂƂ���������͂ɂ��C���F�u�h�E���ۂ��ł��p�x�������C�����MRSA17.5%�C���`�V���������F�u�h�E���ہimethicillin-sensitive S.aureus : MSSA�j6.5%�ł������D�����ŗΔ^�ۂ�13.9%�Ƒ����C�ȏ�̂Q�ێ킪��v���o�ۂł������D 2. �@���x���f�Â̗��� �@���x���̐f�f�ł͖�f�C�g�̏����C���t���������C����X���ʐ^��葍���I�ɔ��f����D��f�ł͊O���C�\ႁC�ċz����Ƃ������ċz��Ǐ�ƁC���M�C���ӊ��C�H�v�s�U�Ƃ������S�g�Ǐ�C�f�@�����ł͋������f�ł�crackles��C���M�C�p���C�p�ċz��F�߂��ꍇ�Ȃǂɔx�����^������X�������C���t�������{�s����D�T�^�I�ȍې��x���ł͋���X�������ł͋C�ǎx���������Z���e��F�߁C���t���������ōD�����D�ʂ̔������������C���ǔ����iCRP�㏸�E�������i�j��F�߂邱�Ƃ�����D�x���̐f�f�ɂ����ẮC���ǂ̏ꂪ�x�����i�x�E�̈�j�ł��邩�C�o�߂͋}���ł��邩�C�������ɂ���Ĉ����N�����ꂽ���ǂł��邩�f���C��ܐ��x���Ȃǂ̔����x���₤�������S�s�S�ȂǂƂ̊ӕʂ��d�v�ł���D 3. �@���x���̎��� HAP�ɂ�����R�ۖ�ɂ�鎡�Ð헪�͑傫���Q�ɕ�������D����̖�܂��g�p���C�S�g��Ԃ̉��P���݂��Ȃ��ꍇ�ɕK�v�ɉ����čL��̖�܂ւ̈ȍ~���l������escalation���ÂƁC�L��̖�܂ŏ������Â��J�n���C�S�g��Ԃ̉��P���m�F���C�\�ł������̖�܂ւ̕ύX���l������de-escalation���Âł���Dde-escalation���Â̓K���ƂȂ�͔̂s���ǁC�d�ǁC�܂��͑ϐ��ۃ��X�N���������҂ł���C�����ɊY�����Ȃ��ꍇ��escalation���Â�I������D���l�x���f�ÃK�C�h���C��2017�ɂ����ẮCHAP�̐f�Âł�I-ROAD�ɂ��d�Ǔx�]�����s�����Ƃ���������Ă���i�}1�j�D�s���ǂ̏�ԁC�d�Ǔx�������ꍇ�C��̓I�ɂ�IROAD�Œ����ǁiB�Q�j�ȏ��HAP�̏ꍇ�C�܂��͑ϐ��ۂ̃��X�N������ꍇ�ɂ́Cde-escalation���Â��s���D�������C�d�Ǔx�ɂ�����炸�Cde-escalation���Â��s���ȕa�Ԃ����݂��邱�Ƃ��l�����Ă����K�v������D���Ȃ킿HAP�͏h���ADL���b�����E�Ɖu�\�ቺ���w�i�ɂ��邱�Ƃ������C�����h��\�͐獷���ʂł���D�܂��K������I-ROAD �ɂ��d�Ǔx�ɉ����ė\�オ�s�ǂɂȂ�Ƃ͌��炸�C�d�Ǔx��������Αϐ��ۂ̕����p�x�������Ƃ������Ƃ��Ȃ��D�܂�D������1,000/��L�������V���Ɖu�s�S�nj�Q�iacquired immunodeficiency syndrome
: AIDS�j���ǎ���Ɖu�}���g�p���̋ɒ[�ȍזE���Ɖu�ቺ��Ԃł�de-escalation���Â��s�킴��Ȃ��ꍇ������C����ɂ͋C�Ǒ}�lj��ɐl�H�ċz��Ǘ����{�s����Ă���Ό뚋����ёϐ��ۂ̉\�����������߁C���Ð����Ƃ��Ă�de-escalation���Â��I������₷���ƌ�����D�t�ɁC�悭�R���g���[�����ꂽ���A�a��y�xCOPD�Ȃǂł͕K������de-escalation���Â��K�v�ł͂Ȃ��D �}1. HAP�̏d�Ǔx����
A. �ϐ��ۃ��X�N�̕]�� HAP�ɂ��ẮC�����ۂɂ��傫�����ÑI�������E����邽�߁C���t�E�\႔|�{�C���ɂ͋C�Njz���t��BAL�t���܂ފe��|�{�����C�v���A���R�������C�a���̂ɑ���y�A�����ł̍R�̌����Ȃǂŋɗ́C�a�ԂɊ֗^����ۂ𖾂炩�ɂ���w�͂����ׂ��ł���D ���l�x���f�ÃK�C�h���C���ł́C�ϐ��ۂ̃��X�N�]���ɂ��āC1. �ߋ�90���ȓ��̌o�Ö��I�R�ۖ�̎g�p���C2. �ߋ�90���ȓ���2���ȏ�̓��@���C3. �Ɖu�}����ԁC4. �������̒ቺ�FPS �� 3�C�o�[�[���w�� < 50�C���s�s�\�C�o�ljh�{�܂��͒��S�Ö��h�{�@��2���ڈȏ�őϐ��ۂ̍����X�N�Q�Ƃ��Ă���D�o�[�[���w���Ƃ́C�H���C�ړ��C���e�C�g�C������C�����C���s�C�K�i���~�C���ւ��C�r�ցC�r�A�ɂ��Ċe�X0〜15�_�ŕ]�����CADL���X�R�A�����O����D
�ϐ��ۃ��X�N�Ȃ��ɂ������Ȍ��o�ہF�x�����ہEMSSA�E�O�����A�������ۉȍہi�N���u�V�G�����E�咰�ۂȂǁj�E�C���t���G���U�ہE���o�������T���� �ϐ��ۃ��X�N����ɂ������Ȍ��o�ہF��L�ɉ����AMRSA�E�Δ^�ہEESBL�Y���ہEAmpC�^��-���N�^�}�[�[�Y���� B. HAP�̃G���s���b�N���� �R�ۖÂ͈�ʓI�ɃG���s���b�N���ÂƕW�I���Âɋ�ʂ����D�G���s���b�N���Â͖{���C�|�{���ʂ���������܂ł̏��������Ԃ̎��ÁC�W�I���Â͕����ۂɑΉ��������ÁC�Ƃ����Ӗ������ŗp������D���������Տ��ł͔|�{�����Ō����ۂ��������Ȃ��ꍇ�������C�������Î��̂��K�C�h���C���̐������W�����ɏ������������̍L�採�Áiempirical broad spectrum antibiotic
treatment�j�ƁC�ʂ̏���v�������@���ʓ������ƂɕW�I��������x�i�����������Áipathogen directed antibiotic
treatment�j�ɋ�ʂ��ĕ��͂��s����ꍇ������D����HAP�ɂ����Ă͑S�g��Ԃ������C����ł���ꍇ���������߁C�\ႂ̔r�o������ŁC���N�P�I�������ł��Ȃ��ǗႪ�����C����������HAP�ł̓G���s���b�N���Â��d�v�ƂȂ�DHAP���҂ł͍���҂�Ɖu�\���ቺ�������҂������C���j�ǂ��郊�X�N���������ґw�ł��邽�߁C���j�����̗L���ɂ��Ă͏\���ɒ��ӂ��C���j�ɑ���R�ۊ�����L����j���[�L�m�����n��̎g�p�͐T�d�ɍs���D a. escalation���� HAP�ł�CAP�Ɣ�r���đϐ��ۃ��X�N���������̂́C�S��őϐ��ۂ�W�I�Ƃ����L��R�ۖ�𓊗^����K�v�͂Ȃ��C�ϐ��ۃ��X�N�C�x���̏d�Ǔx�Ȃǂ��炻�̓K���f����D�K�C�h���C���ł́C�Ք������̌뚋���x���̃��X�N�⎾���I������V���̏�ԂłȂ��ꍇ�C���̃X�e�b�v�Ƃ��đO�q��IROAD�̃t���[�`���[�g�Ȃǂŏd�Ǔx�Ƒϐ��ۃ��X�N�f����悤�L�ڂ���Ă���D�y�njQ��HAP�ŁC���ϐ��ۃ��X�N���Ⴂ�ꍇ�Cescalation���Ái�܂�����X�y�N�g�����̍R�ۖ�𓊗^���C�������̏ꍇ�ɍL��X�y�N�g�����̍R�ۖ��escalation������j�ɂ�鏉�����Â����������Descalation���ÂŕW�I�Ƃ���͔̂x�����ہCMSSA�C�C���t���G���U�ہC���o�������T���ہC�N���u�V�G�����i��ESBL�Y���ہj�C�����N�Z�����Ȃǂ̋ۂł���D�����̋ۂɑ���G���s���b�N���ÂƂ��Đ��������̂́C�y�j�V�����n��ł̓X���o�N�^���E�A���s�V�����C�Z�t�F���n��ł͑�O����̃Z�t�g���A�L�\���܂��̓Z�t�H�^�L�V���C�ے�`�x���̉\��������ꍇ��C��-���N�^���n��̃A�����M�[����L����ꍇ�ɂ̓j���[�L�m�����n��̃��{�t���L�T�V�������������D�O�����Â��\�ȏꍇ�́C������ōې��C���^�x���̗��҂��J�o�[����悤�Ƀ�-���N�^�}�[�[�j�Q��z���y�j�V�����n��i�A���L�V�V�����E�N���u�����_�܂��̓X���^�~�V�����j�C�Z�t�g���A�L�\���Ƀ}�N�����C�h�n��i�N�����X���}�C�V���܂��̓A�W�X���}�C�V���j�p���邩�C���X�s���g���[�L�m�����i�K���m�L�T�V���C���L�V�t���L�T�V���C���{�t���L�T�V���C�V�^�t���L�T�V���C�g�X�t���L�T�V���j��I������D�O���Œ��˖�ɂ�鎡�Â��s���ꍇ�ɂ�1��1�^���\�ȃZ�t�g���A�L�\����{�t���L�T�V����I������D���{�t���L�T�V���͌��C���ۂւ̍R�ۊ������s�\���ł��邽�߁C�뚋���x����x�^ᇁC�x���^�ǂƍs�������C���ۊ����̉\���������Ƃ����a�Ԃł́C�N�����_�}�C�V����g���j�_�]�[���̕��p����������D��������w�a�@������}�j���A���ɁC��\�I�ȃO�����z�����ہC�O�����A�����ۂɂ��ĉ@���̃A���`�o�C�I�O�������f�ڂ���Ă���̂ŁC�ϋɓI�Ɋ��p���ꂽ���D b. de-escalation���� HAP�Ɛf�f����C�s���ǁC�����Ljȏ�̏d�Ǔx�C�܂��͑ϐ��ۂ̃��X�N�������Ɣ��f���ꂽ�Q�ɑ��Ă�de-escalation���Ái�L��̖�܂ŏ������Â��J�n���C�\�ł������̖�܂ւ̕ύX���l�����鎡�Áj��I������D���̌Q�̏������ÂƂ��Ă�escalation���ÌQ�̌����������ɉ����C�ϐ��ہiMRSA�C�Δ^�ہCESBL�Y�������ۂȂǁj���J�o�[����K�v������D �d�Ǔx�������Ɣ��f�����C�܂��͑ϐ��ۂ̃��X�N�������Q�ɑ��Ă�de-escalation�P���Â����������D�R�ۖ�͗Δ^�ۂɍR�ۊ�����L�����-���N�^���n�R�ۖ�Ƃ��ăy�j�V�����n��C��l����Z�t�F���n��C�J���o�y�l���n��C�j���[�L�m�����n��̒P�ܓ��^�����������D �d�Ǔx�������Ɣ��f�����C���ϐ��ۂ̃��X�N�������Q�ɑ��Ă�de-escalation�����Â����������D�R�ۖ�͗Δ^�ۂɍR�ۊ�����L�����-���N�^���n�R�ۖ�Ƃ��ăy�j�V�����n��C��l����Z�t�F���n��C�J���o�y�l���n����x�[�X�ɁC�j���[�L�m�����n��܂��̓A�~�m�O���R�V�h�n��p����D�䂪����HAP�ɐ�߂���^�a���́i�x���}�C�R�v���Y�}�C�N���~�W�A���C���W�I�l���E�j���[���t�B���j�̕p�x�͒Ⴂ���C�����������C�摜�����Ȃǂ�����^�a���̂̊֗^���^����ۂɂ̓j���[�L�m�����n���I������D�܂��CMRSA���������ꂽ����������ꍇ�C�܂��́C�ߋ�90���ȓ��̌o�Ö��I�R�ۖ�̎g�p��������ꍇ��MRSA�����̃��X�N�������Ɣ��f����C�RMRSA��p����D�R�ۖ�̗L������48〜72���Ԍ�ɗՏ��Ǐ�C���t�f�[�^�C�摜�����Ȃǂ��瑍���I�ɔ��肷��D�������Â͑z�肳��錴�����������J�o�[���邽�߂ɍL��ȍR�ۖ�p���邪�C���R�Ǝg�p���邱�Ƃ͑ϐ��ۂ̎Y���C��Ô�̍����̌����ƂȂ�D�܂��R�ۖ�̕���p�ɂ�肩�����ė\��s�ǂƂȂ�Ƃ̕�����C�����������������������_�ł�苷��ȕW�I���Âɐ�ւ���ide-escalation���Áj�D�R�ۖƂ̓��^�ʂ́C�N��C�t�@�\�ɂ���Ē�������D c. HAP�̍R�ۖ^���� �R�ۖ�̓��^���Ԃɂ��ẮC�Z���ԍR�ۖÁi8���ȓ��j�ƒ����Ԏ��Ái10〜15���j���r�������^�A�i�����V�X�̌��ʂł́C�����\��C�������Ì��ʁC���@���ԁC�ĔR�̂�����̃A�E�g�J���ɑ��Ă��L�Ӎ��͎�����Ȃ������D���l�x���f�ÃK�C�h���C���ɂ��C�R�ۖ�̓��^���Ԃ�1�T�Ԉȓ��̔�r�I�Z���Ԃ̎��Ê��Ԃ���Ă���Ă���D���F�u�h�E���ہC�N���u�V�G�����C���C���ۂȂǂɂ��^ᇐ��a�ς�����ꍇ��2�T�Ԉȏ�̒������^���K�v�ł���D �}2. HAP�̃G���s���b�N���ÍR�ۖ�
d. �R�ۖ����̍l���� �x���̏������Âւ̔������s�ǂƔ��f���ꂽ�ꍇ�ɂ́C�a�Ԃ̌������Ǝ��Õ��j�̍Č������C�ꍇ�ɂ���Ă͌�����lj����ď��̎��W���K�v�ƂȂ�D����ł͍R�ۖ�̕ύX���܂���������邱�Ƃ��������C�������Âւ̔����s�ǂɂ͑��ɂ��l�X�Ȉ��q���֗^�����邽�߁C���������q�����łȂ������̈��q�ɂ����ڂ��ď������f�̑Ó������������Ă݂邱�Ƃ��K�v�ł���D�������Õs�����̊ӕʐf�f�̊������̕a�ԂƔ����̕a�Ԃ̗��\�Ɏ����D
C. �l�H�ċz��֘A�x�� a. �Տ��I�E�u�w�I���� �l�H�ċz��֘A�x���iventilator-associated pneumonia :
VAP�j�́C�C�Ǒ}�lj��l�H�ċz���J�n����48���Ԉȍ~�ɐV���ɔ�������HAP���w���DVAP���ǂ̃��X�N���q�͒����l�H�ċz�Ǘ��C�đ}�ǁC���ǑO�̍R�ۖ^�C�������i�M���C�O���C�����_�o�����C�ċz�펾���C�S�����j�C�������邢�͕s�����뚋�C��ʂȂǂł���D���̑�VAP���ǂɂ͋t���C�뚋�C�蒅�i�R���j�[�[�V�����j���֗^����D�ݓ��e���̋t���C���o����C�ǃ`���[�u�ւ̕a���������̒蒅�C�C�ǃ`���[�u�̃J�t�O����������剺�̕��啨�̌뚋�C�l�H�ċz�Ɋ֘A�����P���˂���я��@�\�ቺ�Ȃǂ���������D ICU�ɂ������v�Ȋ����������ǂł���C�ɂ��قȂ邪�C�S�}�NJ��҂�9〜27%�ɔ�������Ƃ����DHAP�ł��邽�߁C���o�ۂƂ��ėΔ^�ۂ��ł������C���̑��G���e���o�N�^�[����X�e�m�g���t�H���i�X���Ȃǂ̎��Ó�a���O�����A�����یQ�CMRSA�Ȃlj��F�u�h�E���ۂ̊����������D b. �f�f �Տ��I�ɇ@�S�g�����ǔ����F���M�CCRP��J���V�g�j���Ȃǂ̏㏸�C�A�_�f���̒ቺ�C�B�摜�����i����X���CCT�C�G�R�[�j��ُ�A�e�̏o���Ǝ����C�C�^���C�����啨���������ꍇ�ȂǂɗՏ��IVAP�Ƃ��Ĕ������w�I�������s���D�������CVAP�͐l�H�ċz���ɐ�����x���ł��邽�߂ɁC��������l�H�ċz�̌����ƂȂ����x�a�ρC���邢�͔x���ȊO�̐l�H�ċz���ɕ������₷���x�a�ρi���C�x�C�����Ȃǁj�Ƃ̊ӕʂ͂�������ł���C���ӂ�v����D VAP�͑}�ǒ��ł���C���̔x���ƈقȂ�a���ւ̃A�N�Z�X���e�Ղȓ��������D�]���ĐϋɓI�ɔ������f�f���s�����Ƃ��\�ł���d�v�ł���D�ȉ��̏ꍇ�C�������w�I�f�f�̖ڈ��Ƃ���D�Ȃ��C��ʔ|�{�͕K�{�ł͂Ȃ��D �@ ���C���̒��ڋz���itracheal aspirate�j�ŕa�����������|�{����C����ʔ|�{3+�ȏ゠�邢�͒�ʔ|�{106CFU/mL�ȏ� �A �C�ǎx�x�E���ibronchoalveolar lavage : BAL�C���邢��mini-BAL�i�C�ǎx���ł͂Ȃ��C�T���v�����O�J�e�[�e���ɂĎ{�s�\�j�ŕa�����������|�{����C����ʔ|�{2+�ȏ゠�邢�͒�ʔ|�{106CFU/mL�ȏ� �B ���t�|�{���邢�͋����|�{���z���ŁC���C������̌��o�������ƈ�v c. ���� VAP�͒v�����̍����a�Ԃł���C����ɑ��ēK�Ȍo���I�R�ۖ��^���ꂽ���ۂ������S���ɉe������DVAP��HAP�̈�a�Ԃł���C�R�ۖ�I����HAP�̂���ɉ����D�R�ۖ�I���ɂ����ẮC�O�����A�����یQ�J�o�[��O��Ƃ��C���ɒ����̓��@��R�ۖÂ̂��銳�҂ł͏�q�̎��Ó�a���O�����A�����یQ�̉\�����l������DMRSA�̊�������ۋہCMRSA�ɖ����ȍR�ۖ�̎g�p���C���C�����̂ł̃O�������F�ŃO�����z�����ۃN���X�^�[�����o�����ꍇ�ɂ́C�RMRSA�p�̕K�v������������D�ϐ��ۂ̔������ɑ��Ƃ��邽�߂ɂ��C�|�{���ʔ�����͉y�I����ւ̍R�ۖ�֕ύX������C�����ǂ��ے�I�ł���Β��~����ide-escalation�j�D d. �\�h VAP�\�h��Ƃ��Ċm���������̂͂Ȃ����C���L�̗\�h��̂������܂Ƃ߂ĉ^�p����o���h���A�v���[�`�����߂��Ă���D �@ ��w�q�� �A ��ʂ̉�� �B �l�H�ċz���H�̕p��̌����̉�� �C �\�Ȓ��Â������ �D �l�H�ċz����̗��E�𑣐i���� �E ���剺�o�z���E�t���`���[�u �F ���o�P�A D. �l�̈ӎv��QOL���l���������ÁE�P�A �ې��x���͈�ʂɍR�ۖ�ɂ���ĕa�������I�Ȏ��Â��\�ł���C��������Α傫�Ȍ��ǂ��c�����ƂȂ��a�O�̏�Ԃɕ��A����ǐ������ł���D����C�s�t�I�Ȏ��̉ߒ��C���Ȃ킿���Ȃǂ̎���������Ԃ�V���̉ߒ��ɂ���l�ɋN�������x���́C���S�̌_�@�ƂȂ�����C�a���P�����Ƃ��Ă��a�O�̏�Ԃɕ��A�ł����C�ނ��늬�����ɂ�s��������������C���邢�͌J��Ԃ��\��������D���̂悤�Ȋ��҂ɑ��ẮC�ߔN�w��̎w�j�ȂǂŏI�����ɂ������Â̌���v���Z�X�ɂ��āC�K�ȏ��̒Ɛ����Ɋ�Â��l�̈ӎv�̑������������悤�ɂȂ��Ă����D �őP�̎��Â��s���Ă������������Ȃ��C���邢�͂킸���ɉ����ł����Ƃ��Ă��{�l�̉��l�ςɏƂ炵�āu�ǂ����X�������v�ƌ�����QOL���ێ��ł��Ȃ��ƁC���m����L���镡���̈�t�ɂ���Ĉ�v���Ĕ��f����銳�҂ɋN�������x���ł́C�l�H�ċz��ɂ��Ǘ���L��R�ۖ��p�������͂Ȏ��Âł͂Ȃ��C�ꂵ�݂��Ƃ�ɘa��Â�D�悵�čs���I���������邱�Ƃ���C�{�l�̈ӎv���m�F���C�{�l�̈ӎv�m�F���ł��Ȃ��ꍇ�ɂ́C�{�l�̈ӎv���悭�m��Ƒ��ɂ�鐄��ӎv�d���C���̈ӎv�ɉ����Ĕx�����Â̊J�n�C�s�J�n�C�I������R�ۖ�̎�ނ𑽐E��ɂ���č\�����ꂽ��Ã`�[���Ƃ��Č��肷��D �f�f���ʂƂ���Ɋ�Â��f�Õ��j�͂��̉ߒ����܂߂Đf�Ø^�ɋL�^����D���̏ꍇ�ł��C�x���ɔ����s�����ɂ���菜���ɘa�I�Ȏ��Â͐ϋɓI�ɗD�悵�čs���ׂ��ł���D����Ɉ�x���肵���f�Õ��j���C�{�l�̊�]�����鎞�ɂ͏ɉ����Ă��ł��ύX�ł��邱�Ƃ��������D |
||||||||||||||||||||||||||||||
|
B.2.4 �����۔������̍R�ۖ�I�� |
||||||||||||||||||||||||||||||
|
�@�\ႂ�p�����ۊw��������ь��t�|�{�����A�A���R�������i�x�����ہA���W�I�l���E�j���[���t�B���j�A�@�����ʂ������̍R�������i�x���}�C�R�v���Y�}�A�C���t���G���U�j�A�\ႍR�������i�x�����ہj�A����IgM�R�̌��o�@�i�x���N���~�W�A�j���ɂ�錴���ۓ���@�Ɋ�Â��A�����ۂ��m�肳�ꂽ�ꍇ�ɂ́A�W�I���Âւ�de-escalation���s���B A) �x������ �@�y�j�V�����ϐ��x�����ۂ̕p�x�͒Ⴂ���A���̏ꍇ�̓��X�s���g���[�L�m��������I���Ƃ���B �O�����Â̏ꍇ�i������j ��P�I��� �EAMPC(���i�V��) �o��(250mg) 1��2�� 1��3〜4��(�Y�t�����ő�4��/��) ��Q�I��� �EGRNX(�W�F�j�i�b�N) �o��1��400mg 1��1�� �EMFLX(�A�x���b�N�X) �o��1��400mg 1��1�� �ELVFX(���{�t���L�T�V��) �o��1��500mg 1��1�� ���@���Â̏ꍇ�i���˖�j ��P�I��� �EABPC(�r�N�V����) �_�H�Ò� 1��1〜2g 1��3〜4�� �EPCG(�y�j�V����) �_�H�Ò� 1��200〜300���P�� 1��4�� ��2�I��� �ECTRX(�Z�t�g���A�L�\��) �_�H�Ò� 1��2g 1��1��܂���1��1g 1��2�� ��R�I��� �ECZOP(�t�@�[�X�g�V��) �_�H�Ò� 1��1〜2g 1��2〜4�� �ECFPM(�}�L�V�s�[��) �_�H�Ò� 1��1〜2g 1��4�� ��S�I��� �EPAPM/BP(�J���x�j��) �_�H�Ò� 1��0.5〜1g 1��2〜4��(�Y�t�����ő�2g/��) �EMEPM(�����y�l��) �_�H�Ò� 1��1g 1��2〜3�� �EDRPM(�t�F�j�o�b�N�X) �_�H�Ò� 1�� 0.5〜1g 1��3�� �EBIPM(�I���K�V��) �_�H�Ò� 1�� 0.3〜0.6g 1��3〜4��(�Y�t�����ő�1.2g/��) �EIPM/CS(�`�G�i��) �_�H�Ò� 1�� 0.5〜1g 1��2〜4��(�Y�t�����ő�2g/��) B) �C���t���G���U�� �@�C���t���G���U�ۑS�̂ɐ�߂��-���N�^�}�[�[��Y���A���s�V�����ϐ��C���t���G���U��(��-lactamase-negative,
ampicillin-resistant H. influenzae
: BLNAR)��18.7%�A��-���N�^�}�[�[�Y���A���L�V�V�����E�N���u�����_�ϐ��C���t���G���U��(��-lactamase-positive amoxicillin/clavulanate resistant H. influenzae : BLPACR)��5.7%�ł��邪�A����ϐ����̕ϓ����\�z�����BBLNAR�͑�ꐢ��Z�t�F���n��A���Z�t�F���n��ɑϐ��ł���B�s�y���V������BLNAR�ɍR�ۗ͂��������ABLPACR�ɂ͖����ł���B�^�]�o�N�^���E�s�y���V�����͗��҂ɗL���ł���BBLNAR�ɂ̓��X�s���g���[�L�m��������I���Ƃ���B �O�����Â̏ꍇ�i������j ���I��� �ESBTPC(���i�V��) �o��(375mg) 1��2�� 1��3〜4��(�Y�t�����ő�3��/��) �ECVA/AMPC(�I�[�O�����`��) �o��(125mg/250mg)
1��2�� 1��3〜4��(�Y�t�����ő�4��/��) ���I��� �EGRNX(�W�F�j�i�b�N) �o��1��400mg 1��1�� �EMFLX(�A�x���b�N�X) �o��1��400mg 1��1�� �ELVFX(���{�t���L�T�V��) �o��1��500mg 1��1�� ���@���Â̏ꍇ�i���˖�j ���I��� �ESBT/ABPC(���i�V���E�X���o�V����) �_�H�Ò� 1��3g 1��3〜4�� ���I��� �ECTRX(�Z�t�g���A�L�\��) �_�H�Ò� 1��2g 1��1��܂���1��1g 1��2�� �ECTX(�N���t�H����) �_�H�Ò� 1��1〜2g 1��2〜3��(�Y�t�����ő�4g/��) �ETAZ/PIPC(�]�V���E�^�]�s�y) �_�H�Ò� 1��4.5g 1��3〜4�� ��O�I��� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �ECPFX(�V�v���L�T��) �_�H�Ò� 1�� 300mg 1��2�� �EPZFX(�p�Y�N���X) �_�H�Ò� 1�� 500〜1000mg 1��2�� C) �N���u�V�G�����A���̒����ۉ� �@Extended spectrum ��-lactamase(ESBL)�Y���ۂ̔䗦�͑����X���ł���A�ċz�팟�̗R���N���u�V�G���̂����AESBL�̊�����1.3%�ł���BESBL�Y�����̑����̓L�m�����ϐ����ɗL���Ă���B �O�����Â̏ꍇ�i������j ���I��� �ESBTPC(���i�V��) �o��(375mg) 1��2�� 1��3〜4��(�Y�t�����ő�3��/��) �ECVA/AMPC(�I�[�O�����`��) �o��(125mg/250mg)
1��2�� 1��3〜4��(�Y�t�����ő�4��/��) ���I��� �EGRNX(�W�F�j�i�b�N) �o��1��400mg 1��1�� �EMFLX(�A�x���b�N�X) �o��1��400mg 1��1�� �ELVFX(���{�t���L�T�V��) �o��1��500mg 1��1�� ���@���Â̏ꍇ�i���˖�j ���I��� �ECTM(�Z�t�H�`�A��) �_�H�Ò� 1��1〜2g 1��2〜3��(�Y�t�����ő�4g/��) �ECTRX(�Z�t�g���A�L�\��) �_�H�Ò� 1��2g 1��1��܂���1��1g 1��2�� �ECTX(�N���t�H����) �_�H�Ò� 1��1〜2g 1��2〜3��(�Y�t�����ő�4g/��) �ESBT/ABPC(���i�V���E�X���o�V����) �_�H�Ò� 1��3g 1��3〜4�� ���I��� �ETAZ/PIPC(�]�V���E�^�]�s�y) �_�H�Ò� 1��4.5g 1��3〜4�� ��O�I��� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �ECPFX(�V�v���L�T��) �_�H�Ò� 1�� 300mg 1��2�� �EPZFX(�p�Y�N���X) �_�H�Ò� 1�� 500〜1000mg 1��2�� D) �x���}�C�R�v���Y�} �@�}�N�����C�h�����}�C�R�v���Y�}�����ǂŊO�����Â��s���ꍇ�́A�}�N�����C�h�n����I���Ƃ���B�}�N�����C�h�n�^��A48〜72���Ԃʼn�M���Ȃ��ꍇ�́A�}�N�����C�h�ϐ��}�C�R�v���Y�}�x�����^���A������A���˖�Ƃ��Ƀ~�m�T�C�N�����𓊗^����B �O�����Â̏ꍇ�i������j ���I��� �ECAM(�N�����X) �o�� 1��200mg 1��2�� �EAZM(�W�X���}�b�N) �������܌o�� 1��2g �P�^ ���I��� �EMINO(�~�m�}�C�V��) �o��1��100mg 1��2�� �EGRNX(�W�F�j�i�b�N) �o��1��400mg 1��1�� �EMFLX(�A�x���b�N�X) �o��1��400mg 1��1�� �ELVFX(���{�t���L�T�V��) �o��1��500mg 1��1�� ���@���Â̏ꍇ�i���˖�j ���I��� �EMINO(�~�m�}�C�V��) �_�H�Ò� 1��100mg 1��2�� �EAZM(�A�W�X���}�C�V��) �_�H�Ò� 1��500mg 1��1�� ���I��� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �ECPFX(�V�v���L�T��) �_�H�Ò� 1�� 300mg 1��2�� E) ���W�I�l���E�j���[���t�B�� �@�d�ǔx���ł̓j���[�L�m�����n��ƃA�W�X���}�C�V���̕��p���ʂ�����������B ���@���Â̏ꍇ�i���˖�j ���I��� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �ECPFX(�V�v���L�T��) �_�H�Ò� 1�� 300mg 1��2�� �EPZFX(�p�Y�N���X) �_�H�Ò� 1�� 500〜1000mg 1��2�� �EAZM(�A�W�X���}�C�V��) �_�H�Ò� 1��500mg 1��1�� F) �N���~�W�A�� �@�זE���ڍs���ǍD�ŁA�������N���~�W�A���B�}����������܂ɂ́A�e�g���T�C�N�����n��A�}�N�����C�h�n��A�j���[�L�m�����n��Ȃǂ�����B �O�����Â̏ꍇ�i������j ���I��� �EMINO(�~�m�}�C�V��) �o��1��100mg 1��2�� ���I��� �ECAM(�N�����X) �o�� 1��200mg 1��2�� �EAZM(�A�W�X���}�C�V��) �������܌o�� 1��2g �P�^ ��O�I��� �EMINO(�~�m�}�C�V��) �o��1��100mg 1��2�� �EGRNX(�W�F�j�i�b�N) �o��1��400mg 1��1�� �EMFLX(�A�x���b�N�X) �o��1��400mg 1��1�� �ELVFX(���{�t���L�T�V��) �o��1��500mg 1��1�� ���@���Â̏ꍇ�i���˖�j ���I��� �EMINO(�~�m�}�C�V��) �_�H�Ò� 1��100mg 1��2�� ���I��� �EAZM(�A�W�X���}�C�V��) �_�H�Ò� 1��500mg 1��1�� ��O�I��� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� G) ���`�V���������F�u�h�E����(MSSA) MSSA�����ǁi�ی��ǁj�̏ꍇ�ɂ̓Z�t�@�]�����̂ق����o���R�}�C�V�������Տ����ʂ������B �O�����Â̏ꍇ�i������j ���I��� �ESBTPC(���i�V��) �o��(375mg) 1��2�� 1��3〜4��(�Y�t�����ő�3��/��) �ECVA/AMPC(�I�[�O�����`��) �o��(125mg/250mg)
1��2�� 1��3〜4��(�Y�t�����ő�4��/��) ���I��� �ECAM(�N�����X) �o�� 1��200mg 1��2�� �EAZM(�A�W�X���}�C�V��) �������܌o�� 1��2g �P�^ ���@���Â̏ꍇ�i���˖�j ���I��� �ESBT/ABPC(���i�V���E�X���o�V����) �_�H�Ò� 1��3g 1��3〜4�� �ECEZ(�Z�t�@�]����) �_�H�Ò� 1��1〜2g 1��2〜3��(�Y�t�����ő�5g/��) ���I��� �EMINO(�~�m�}�C�V��) �_�H�Ò� 1��100mg 1��2�� �ECLDM(�N�����_�}�C�V��) �_�H�Ò� 1��600mg 1��2〜4�� H) ���`�V�����ϐ����F�u�h�E����(MRSA) �O�����Â̏ꍇ�i������j ���I��� �ELZD(�U�C�{�b�N�X) �o�� 1��600mg 1��2�� ���@���Â̏ꍇ�i���˖�j ���I��� �EVCM(�o���R�}�C�V��) �_�H�Ò� 1��1g(�܂���15mg/kg) 1��2�� �ETEIC(�e�C�R�v���j��) �_�H�Ò� 2����1��400mg 1��2�[�f�B���O�A3���ڈȍ~1��400mg 1��1��(�Y�t�����ő� 800mg �����A�ȍ~400mg/��) �ELZD(�U�C�{�b�N�X) �_�H�Ò� 1��600mg 1��2�� I) �����T���� �O�����Â̏ꍇ�i������j ���I��� �EAMPC(�r�N�V����) �o��(250mg) 1��2�� 1��3〜4��(�Y�t�����ő�4��/��) �EAZM(�A�W�X���}�C�V��) �������܌o�� 1��2g �P�^ ���I��� �ESBTPC(���i�V��) �o��(375mg) 1��2�� 1��3〜4��(�Y�t�����ő�3��/��) �ECVA/AMPC(�I�[�O�����`��) �o��(125mg/250mg)
1��2�� 1��3〜4��(�Y�t�����ő�4��/��) ��O�I��� �EGRNX(�W�F�j�i�b�N) �o��1��400mg 1��1�� �EMFLX(�A�x���b�N�X) �o��1��400mg 1��1�� �ELVFX(���{�t���L�T�V��) �o��1��500mg 1��1�� ���@���Â̏ꍇ�i���˖�j ���I��� �EABPC(�r�N�V����) �_�H�Ò� 1��1〜2g 1��3〜4�� �EPCG(�y�j�V����) �_�H�Ò� 1��200〜300���P�� 1��4�� �EAZM(�A�W�X���}�C�V��) �_�H�Ò� 1��500mg 1��1�� ���I��� �ESBT/ABPC(���i�V���E�X���o�V����) �_�H�Ò� 1��3g 1��3〜4�� �ETAZ/PIPC(�]�V���E�^�]�s�y) �_�H�Ò� 1��4.5g 1��3〜4�� J) �����N�Z���E�J�^���[���X �O�����Â̏ꍇ�i������j ���I��� �ESBTPC(���i�V��) �o��(375mg) 1��2�� 1��3〜4��(�Y�t�����ő�3��/��) �ECVA/AMPC(�I�[�O�����`��) �o��(125mg/250mg)
1��2�� 1��3〜4��(�Y�t�����ő�4��/��) ���I��� �ECAM(�N�����X) �o�� 1��200mg 1��2�� �EAZM(�A�W�X���}�C�V��) �������܌o�� 1��2g �P�^ ��O�I��� �EGRNX(�W�F�j�i�b�N) �o��1��400mg 1��1�� �EMFLX(�A�x���b�N�X) �o��1��400mg 1��1�� �ELVFX(���{�t���L�T�V��) �o��1��500mg 1��1�� ���@���Â̏ꍇ�i���˖�j ���I��� �ESBT/ABPC(���i�V���E�X���o�V����) �_�H�Ò� 1��3g 1��3〜4�� ���I��� �ECTM(�Z�t�H�`�A��) �_�H�Ò� 1��1〜2g 1��2〜3��(�Y�t�����ő�4g/��) �ECTRX(�Z�t�g���A�L�\��) �_�H�Ò� 1��2g 1��1��܂���1��1g 1��2�� �ECTX(�N���t�H����) �_�H�Ò� 1��1〜2g 1��2〜3��(�Y�t�����ő�4g/��) ��O�I��� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �ECPFX(�V�v���t���L�T�V��) �_�H�Ò� 1�� 300mg 1��2�� �EPZFX(�p�Y�N���X) �_�H�Ò� 1�� 500〜1000mg 1��2�� K) ���C���� �O�����Â̏ꍇ�i������j ���I��� �ESBTPC(���i�V��) �o��(375mg) 1��2�� 1��3〜4��(�Y�t�����ő�3��/��) �ECVA/AMPC(�I�[�O�����`��) �o��(125mg/250mg)
1��2�� 1��3〜4��(�Y�t�����ő�4��/��) ���I��� �EGRNX(�W�F�j�i�b�N) �o��1��400mg 1��1�� �EMFLX(�A�x���b�N�X) �o��1��400mg 1��1�� �ESTFX(�s�̗p) �o��1��100mg 1��1〜2�� ���@���Â̏ꍇ�i���˖�j ���I��� �ESBT/ABPC(���i�V���E�X���o�V����) �_�H�Ò� 1��3g 1��3〜4�� ���I��� �EMNZ(�A�l���g��) �_�H�Ò� 1�� 500mg 1��3〜4�� �ECLDM(�N�����_�}�C�V��) �_�H�Ò� 1�� 600mg 1��2〜4�� L) �Δ^�� �O�����Â̏ꍇ�i������j ���I��� �ELVFX(���{�t���L�T�V��) �o��1��500mg 1��1�� �ESTFX(�s�̗p) �o��1��100mg 1��1〜2�� �ECPFX(�V�v���t���L�T�V��) �o�� 1�� 200mg 1��3�� ���@���Â̏ꍇ�i���˖�j ���I��� �EPIPC(�y���g�V����) �_�H�Ò� 1��2〜4g 1��4��(�Y�t�����ő�8g/��) �ETAZ/PIPC(�]�V���E�^�]�s�y) �_�H�Ò� 1��4.5g 1��3〜4�� ���I��� �ECAZ(�Z�t�^�^�W��) �_�H�Ò� 1��1〜2g 1��4��(�Y�t�����ő�4g/��) �ECZOP(�t�@�[�X�g�V��) �_�H�Ò� 1��1〜2g 1��2〜4�� �ECFPM(�}�L�V�s�[��) �_�H�Ò� 1��1〜2g 1��4�� ��O�I��� �ELVFX(���{�t���L�T�V��) �_�H�Ò� 1�� 500mg 1��1�� �ECPFX(�V�v���t���L�T�V��) �_�H�Ò� 1�� 300mg 1��2�� �EPZFX(�p�Y�N���X) �_�H�Ò� 1�� 500〜1000mg 1��2�� ��l�I��� �EMEPM(�����y�l��) �_�H�Ò� 1��1g 1��2〜3�� �EDRPM(�t�F�j�o�b�N�X) �_�H�Ò� 1�� 0.5〜1g 1��3�� �EBIPM(�I���K�V��) �_�H�Ò� 1�� 0.3〜0.6g 1��3〜4��(�Y�t�����ő�1.2g/��) |
||||||||||||||||||||||||||||||
|
�Q�l���� |
||||||||||||||||||||||||||||||
|
�E���{�ċz��w��@���l�x���f�ÃK�C�h���C��2017 �E���{�����NJw��E���{���w�Ö@�w��@�����ǎ��ÃK�C�h2014 �E���{���w�Ö@�w��E���{�����NJw��@MRSA�����ǂ̎��ÃK�C�h���C���i2013�N6�����s�j |