臨床研究部門(利益相反審査委員会)
治験審査委員会に関するご案内はこちら
▶治験審査委員会(治験管理部門)
▶治験審査委員会(治験管理部門)
臨床研究管理センターに関するご案内はこちら
▶トップページ
▶トップページ
利益相反審査委員会に関するご案内はこちら
▶トップページ
▶関連規則
▶利益相反審査委員
▶鹿児島大学病院における臨床研究に係る利益相反管理について
▶利益相反審査申請様式(自己申告書)
▶利益相反自己申告書の提出手順(臨床研究)
▶利益相反自己申告書の提出手順(治験:製造販売後臨床試験)
▶各委員会に関するお問合わせ
▶トップページ
▶関連規則
▶利益相反審査委員
▶鹿児島大学病院における臨床研究に係る利益相反管理について
▶利益相反審査申請様式(自己申告書)
▶利益相反自己申告書の提出手順(臨床研究)
▶利益相反自己申告書の提出手順(治験:製造販売後臨床試験)
▶各委員会に関するお問合わせ
利益相反自己申告書の提出手順(治験:製造販売後臨床試験)
提出対象者
企業治験および医師主導治験に関わる治験責任医師および治験分担医師 全員
申告の範囲
申告者とその家族※
※申告者と収入や財産を共有する立場にある配偶者及び生計を一にする扶養家族
申告する対象期間
申告日より起算して,過去1年間の活動・報酬について
提出書類
- 臨床研究に係る利益相反自己申告書(概略)
- 臨床研究に係る利益相反自己申告書(詳細)(1つでも「有」がある場合に提出)
- 治験実施計画書 1部
- 同意説明文書
★ 3.及び4. については、治験管理部門にて準備し、提出いたします★
提出方法
各治験の治験責任医師がすべてとりまとめの上、提出して下さい。
★個人情報保護のため、提出の際は厳封してください★
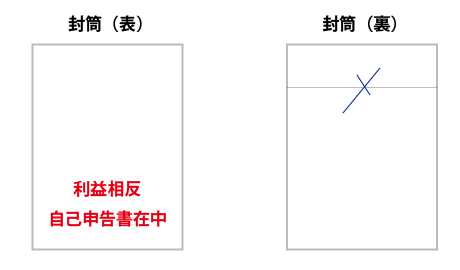
提出先
利益相反審査委員会事務局(臨床研究管理センター)
提出期限
審査予定IRB開催月の前月第2週金曜日までに提出して下さい。
注意事項
提出期限に間に合わないと、IRB審議に影響します。必ず提出期限までにご提出下さい。
利益相反に関するお問い合わせ先
鹿児島大学病院 利益相反審査委員会事務局
TEL:099-275-6624(FAX:099-275-6626)
E-Mail:このメールアドレスはスパムボットから保護されています。閲覧するにはJavaScriptを有効にする必要があります。

 HOME
HOME 病院紹介
病院紹介 受診される方へ
受診される方へ 医療関係者の方へ
医療関係者の方へ 診療科案内
診療科案内 部門案内
部門案内 よくある質問
よくある質問 お問合せ
お問合せ アクセス・駐車場
アクセス・駐車場


