臨床研究管理センターとは
治験審査委員会に関するご案内はこちら
臨床研究を始める前に
『鹿児島大学』のIRBを利用する生命科学・医学系研究
『外部機関』のIRBを利用する生命科学・医学系研究
その他の公開情報
臨床研究法関連
「人を対象とする生命科学・医学系研究に関する倫理指針」について
人を対象とした医学系研究を行う場合、文部科学省並びに厚生労働省の定める「人を対象とする生命科学・医学系研究に関する倫理指針」に基づき実施することになります。本学ではこの指針に基づいて、倫理審査委員会を開催しています。
- ⚠倫理審査委員会の審査を受けて承認後、研究機関長による実施許可を得るまで研究を開始する事ができません。
人を対象とする生命科学・医学系研究に関する倫理指針・ガイダンス
🔍研究に関する指針について |厚生労働省 (mhlw.go.jp)
🔍人を対象とする生命科学・医学系研究 |文部科学省 (mext.go.jp)
指針では倫理審査の実務やチェックポイントが示されており、計画書の作成にも役立ちます。下記の事項は申請の際、確認しておきたい事項です。
- 第1章第2 用語の定義
📖「生命科学・医学系研究」など重要用語の意味。 - 第1章第3 適用範囲
📖どんな研究がこの指針の対象になるか。 - 第3章第6 研究計画書に関する手続
📖審査の流れと研究実施許可や研究の事前公開。 - 第3章第7 研究計画書の記載事項
📖計画書の作成方法や審査の流れ。 - 第4章第8 インフォームド・コンセントを受ける手続き等
📖研究参加者に対する説明・同意のあり方。
臨床研究倫理委員会・疫学研究等倫理委員会の委員会情報
研究者等から申請のあった生命科学・医学系研究の実施計画の倫理的妥当性等について審査をするため、鹿児島大学桜ヶ丘地区には次の倫理審査委員会が設置されています。
倫理審査委員会の正式名称
➤鹿児島大学桜ヶ丘地区臨床研究倫理委員会
Ethics Committee on Clinical Research, Sakuragaoka Campus, Kagoshima University
➤鹿児島大学桜ヶ丘地区疫学研究等倫理委員会
Ethics Committee on Epidemiological and its related Studies, Sakuragaoka Campus, Kagoshima University
運営規則・公開情報等
📝鹿児島大学桜ヶ丘地区における人を対象とする生命科学・医学系研究に関する倫理規則
📝国立大学法人鹿児島大学が保有する個人情報の保護管理に関する規則
審査手数料等の設定
臨床研究倫理委員会・疫学研究等倫理委員会への審査依頼に係る審査手数料は設定されておりません。
会議記録の概要
🔍研究倫理審査委員会報告システム(厚生労働省)から記録の概要をご確認ください。
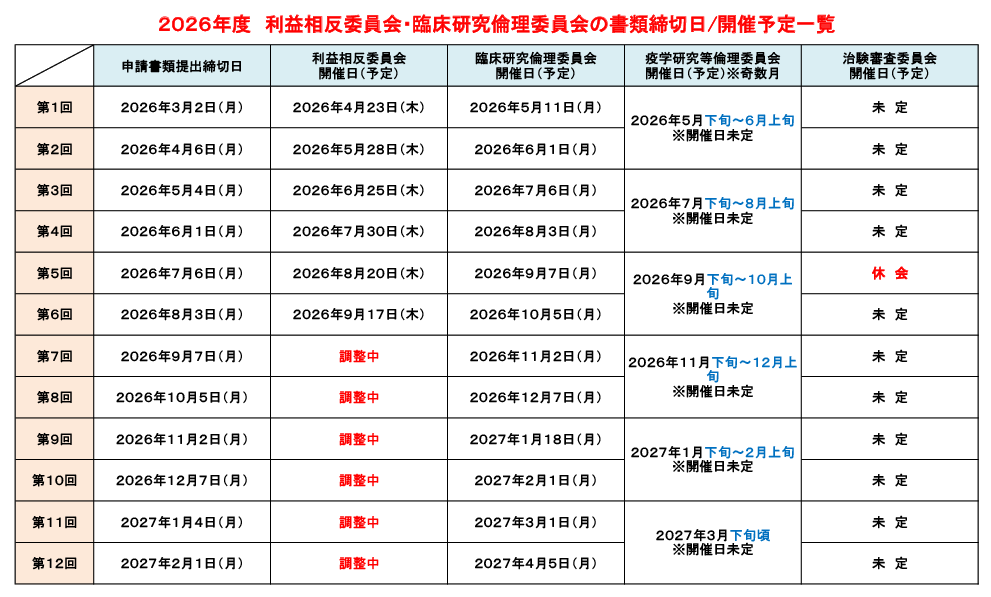
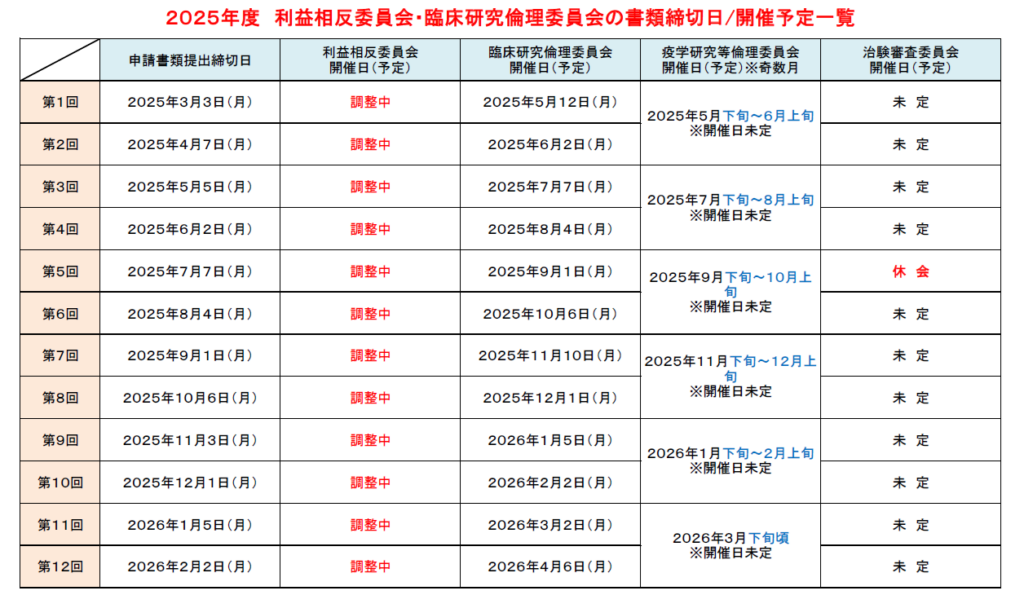
2025年度 利益相反委員会・臨床研究倫理委員会の書類締切日/開催予定
書類締切日/開催予定のご案内
利益相反委員会および臨床研究倫理委員会の 書類提出締切日 および 開催予定 は下記の通りです。
提出期限までに必要書類をご準備のうえ、ご提出ください。
📌利益相反委員会の開催日:原則として毎月第3木曜日
📌臨床研究倫理委員会の開催日:原則として毎月第1月曜日
(委員の都合等により変更される場合があります。)
- ⚠委員会開催スケジュールを確認の上、余裕を持って申請してください。
- ⚠未受講者や書類の不備のある申請は、不備が解消された直近の締切日にて受理、手続き開始となります。
【治験審査委員会へ新規治験を申請する治験責任医師及び治験分担医師の先生へ】
自己申告書(概要)(全員)及び自己申告書(詳細)(該当者のみ)を治験責任医師が取りまとめのうえ、臨床研究管理センターにご提出ください。ご不明点は、治験管理部門・担当CRCまでお問い合わせください。
| こちらよりPDFダウンロード可能です。 |
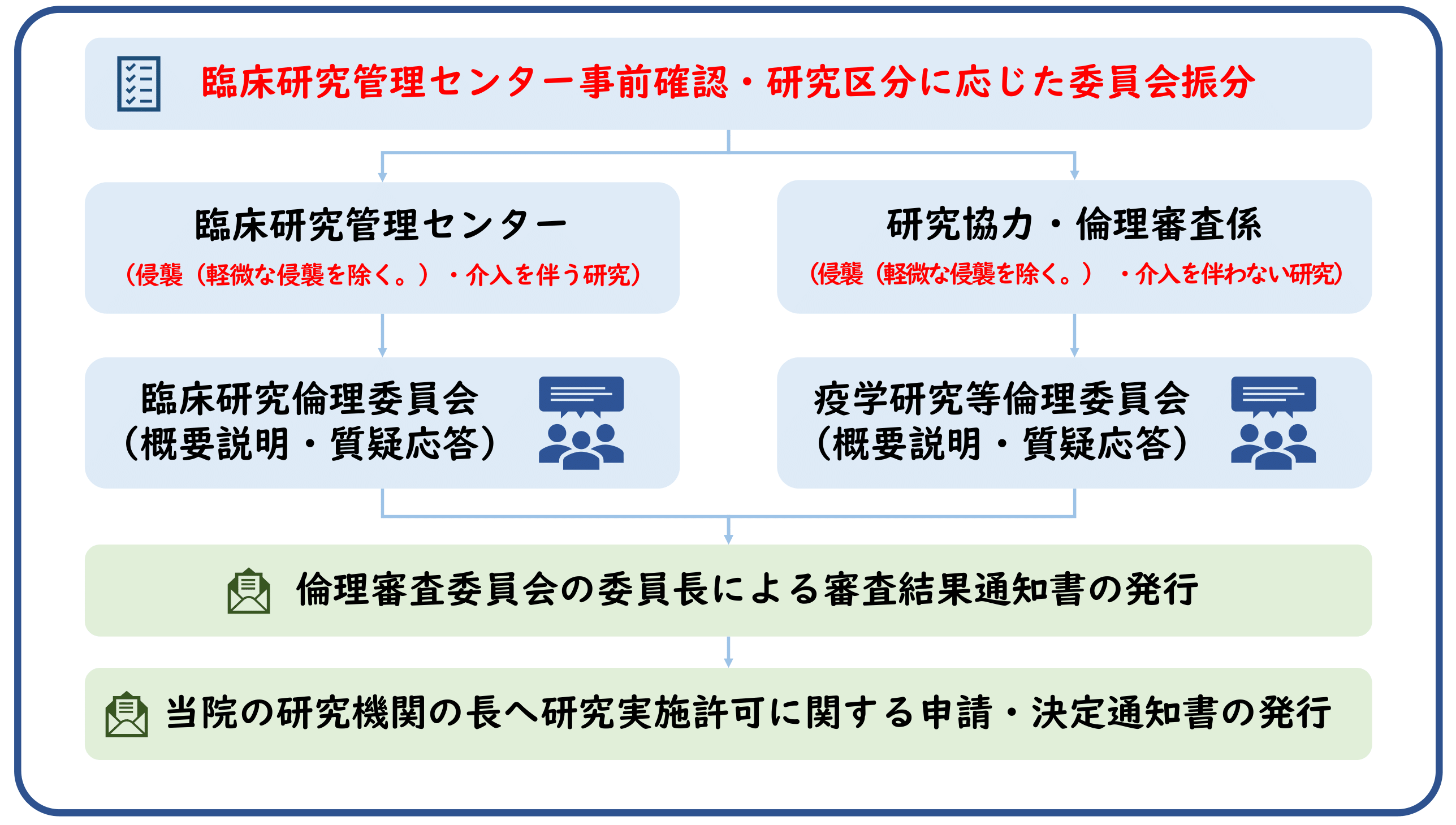
臨床研究倫理委員会・疫学研究等倫理委員会への新規審査依頼
新規審査依頼
研究責任者(多機関共同研究の場合は研究代表者)は、研究を実施しようとするときは、あらかじめ研究計画書等を作成し、実施の適否について倫理審査委員会に意見を聴く必要があります。研究責任者(多機関共同研究の場合は研究代表者)は、申請に必要な書類を揃え、臨床研究管理センターへお申込みください。
■提出先:臨床研究管理センター(crmc@m2.kufm.kagoshima-u.ac.jp)
📌申請書類一式は臨床研究管理センター宛てに電子メールで送信願います。
📌利益相反自己申告書(概略)及び利益相反自己申告書(詳細)は署名捺印の上で学内便で送付願います。
『複数の共同研究機関が参加する多機関共同研究』を一括して審査を行う場合、各施設毎に下記書類が必要です:
1.研究者等リスト
2.研究分担機関の確認書
3.研究機関要件確認書💡提出は 各施設ごとに必ず揃える必要があります。
💡「一括審査=まとめて審査する」場合でも、施設ごとの書類は必須です。
💡多機関共同研究の研究計画書を申請しようとする研究代表者が留意すべき事項を参照下さい。🎯介入研究の申請に関する重要な注意事項
介入研究は倫理審査が特に厳格です。書類不備や記載不足がある場合、申請は差し戻されることがあります。
➤以下のチェックシートや参考資料を必ず確認してください。
📝介入研究の倫理審査依頼時のチェックシート【申請者用】
🔍委員会の審査の視点(厚生労働省)
➤以下の点を必ず確認して、論理的に説明されているかを確認してください。
🔵主要評価項目・研究デザイン
評価項目が主観的で曖昧/デザインが論理的に矛盾する/比較群や割付方法が記載不十分の場合など
🔵症例数の設定根拠・統計学的考察
症例数の算出根拠(有意水準・検出力・想定する効果量)や主解析方法が記載不十分の場合など
❌差し戻しになりやすい記載例
・「有効性を評価する」だけ(測定時期・研究スケジュール・具体的尺度が不明。)
・「先行研究を参考にXX例とした」だけ(根拠の出典・臨床的意味のある差・効果量の説明・SDの記載なし。)
・「統計解析を行う」とだけ(統計解析の手法・検定条件が不明で再現性・透明性なし。)
生命科学・医学系指針 第6 研究計画書に関する手続 2 倫理審査委員会への付議
- 研究責任者は、研究の実施の適否について、倫理審査委員会の意見を聴かなければならない。
- 研究代表者は、原則として、多機関共同研究に係る研究計画書について、一の倫理審査委員会による一括した審査を求めなければならない。
- 研究責任者は、倫理審査委員会に意見を聴いた後に、その結果及び当該倫理審査委員会に提出した書類、その他研究機関の長が求める書類を研究機関の長に提出し、当該研究機関における当該研究の実施について、許可を受けなければならない。
新規審査依頼の流れ
新規審査依頼の書式一覧
| 提出書類(※提出先:crmc@m2.kufm.kagoshima-u.ac.jp) ※利益相反自己申告書は学内便で提出ください。 |
書式 | 参考記載例 |
| 生命科学・医学系研究倫理審査申請書(新規) ・倫理指針に基づく研究の新規審査依頼時に使用します。 ・研究責任者が作成して、IRBに提出します。 |
WORD | 疫学研究 ●ケースコントロール 介入研究 ●クロスオーバー |
| 研究者等リスト ・研究機関毎に、研究責任者と研究分担者を示すこと。 ・鹿児島大学のIRBにて審査対象となる機関毎に作成が必要。 例:一括審査(代表+分担C大学) ★代表:鹿児島大学:研究者等リスト(鹿大) ◎分担(C大学) 研究者等リスト、研究分担機関の確認書、研究機関要件確認書 |
WORD | 例1:単施設(鹿大のみ) 例2:多機関共同研究 ★代表:鹿児島大学 ◎分担:C大学 |
| 研究分担機関の確認書 ・鹿児島大学以外の施設を含む審査を依頼する際に、機関毎に作成。 |
WORD | 例:多機関共同研究 ◎分担:C大学 |
| 研究機関要件確認書 ・鹿児島大学以外の施設を含む審査を依頼する際に、機関毎に作成。 ・各機関の利益相反管理や研究の教育・研修は、各施設の規定に従う。 ※各施設の総務課や臨床研究部門にも支援を頂くこと。 |
WORD | 例:多機関共同研究 ◎分担:C大学 |
| 生命科学・医学系研究実施計画書 ・主要評価項目、デザイン、症例数設計を具体的に記載下さい。 ・必要に応じ、事前の生物統計家によるコンサルを推奨します。 ・任意の様式でご作成いただくことでも構いません。 |
WORD | 疫学研究 ●ケースコントロール 介入研究 ●クロスオーバー |
| 情報公開文書 ・侵襲・介入がなく新たな試料取得を行わない研究が対象。 ・本人同意が困難(例.転居・連絡先なし等)である場合に 該当するかを検討の上、IC手続きを検討下さい。 |
WORD | 疫学研究 ●ケースコントロール |
| 説明文書・同意書・同意撤回通知書 ・専門用語は注釈を入れて、理解できる言葉を使用下さい。 ・目安として6~12歳(小学生)はアセント文書を用意下さい。 ・施設毎の固有情報(施設名や連絡先など)は、記載変更を 認める箇所として注釈や赤字などでお示し下さい。 |
WORD | 介入研究 ●クロスオーバー |
| 研究実施許可願の申請書 ・新規・変更の審査依頼の際に、併せてご提出ください。 ・介入研究は病院長/観察研究は研究科長の実施許可を 取得願います。 |
WORD | 疫学研究 ●ケースコントロール 介入研究 ●クロスオーバー |
| 利益相反自己申告書(概要) ・学内研究者毎に、署名捺印して学内便で提出下さい。 ・個人的COIの有無:年間合計200万円以上が目安。 ・組織的COIの有無:年間合計100万円以上が目安。 |
WORD | 例:企業の関与なし |
| 利益相反自己申告書(詳細) ・学内研究者毎に、署名捺印して学内便で提出下さい。 ・申告書(概要)にてCOI「有」の場合、提出下さい。 |
WORD | ー |
| その他の資料(※該当する場合) ・被験者の募集に関する手順や募集広告等の資料 ・臨床研究保険の見積依頼書(参考:国大協サービス) ・医薬品等の概要を記載した書類(最新版の添付文書など) ・モニタリングに関する手順書 ・監査に関する手順書 |
- | - |
新規審査依頼の提出書類

項1~4に該当する研究は直下の案内を参照して提出書類をダウンロード願います。
項5~8に該当する研究の提出書類はこちらを参照願います。
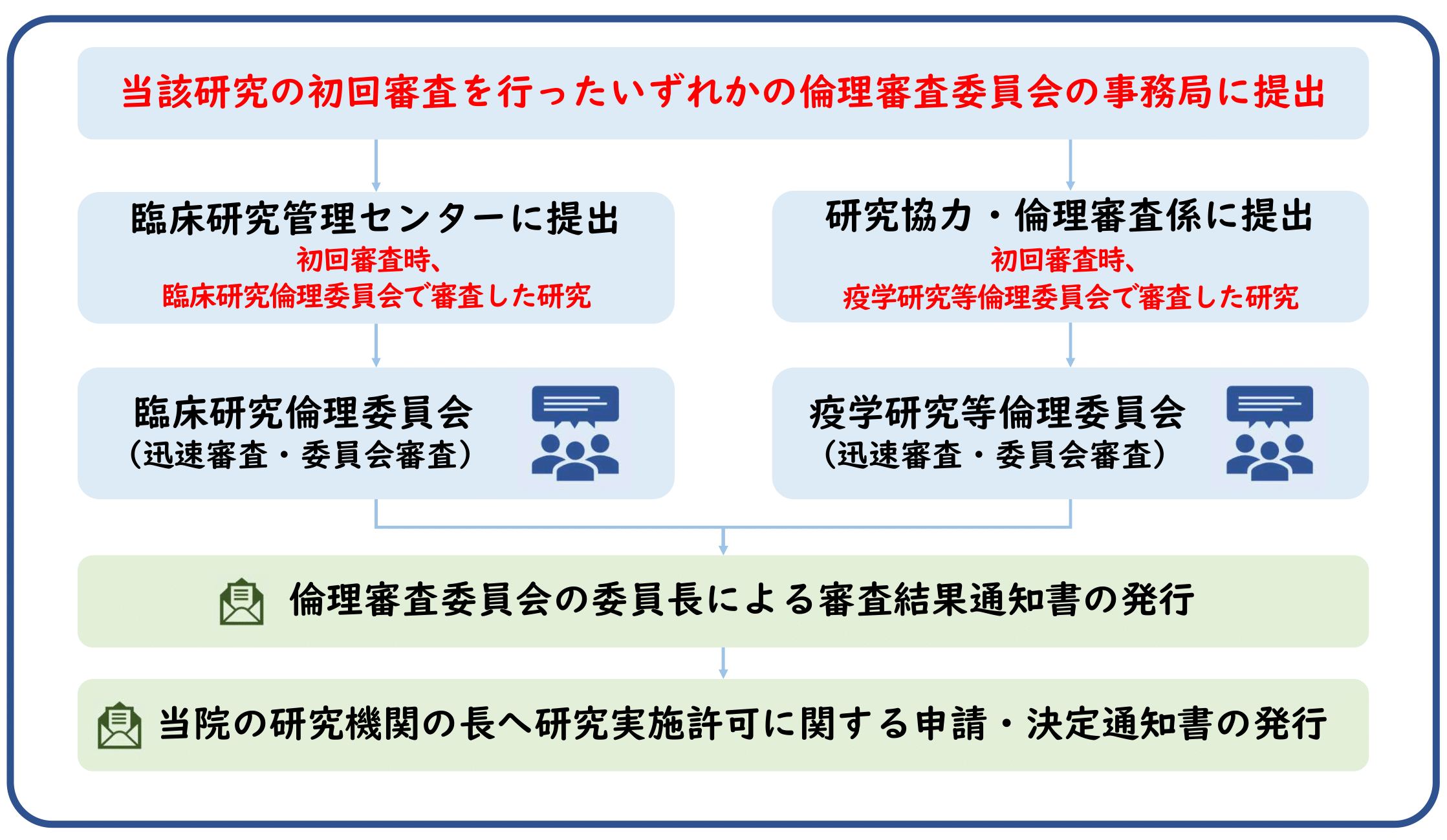
臨床研究倫理委員会・疫学研究等倫理委員会への変更審査依頼
研究責任者(多機関共同研究の場合は研究代表者)は、倫理審査委員会の審査対象となる文書が追加、更新又は改訂された場合、継続の適否について倫理審査委員会に意見を聴く必要があります。研究責任者(多機関共同研究の場合は研究代表者)は、申請に必要な書類を揃え、当該研究の初回審査を行ったいずれかの倫理審査委員会の事務局へお申込みください。
■初回審査時、臨床研究倫理委員会で審査した研究
📌提出先:臨床研究管理センター(crmc@m2.kufm.kagoshima-u.ac.jp)
📌提出方法:申請書類一式を電子メールで送信
📌利益相反自己申告書(概略・詳細):学内便で送付
■初回審査時、疫学研究等倫理委員会で審査した研究
📌提出先:研究協力・倫理審査係(isgskkrs@kuas.kagoshima-u.ac.jp)
鹿児島大学桜ヶ丘地区疫学研究等倫理委員会 | 鹿児島大学大学院 医歯学総合研究科
📌提出方法:申請書類一式を電子メールで送信
変更審査依頼の流れ
変更審査依頼の提出書類
| 提出書類一覧 |
| 生命科学・医学系研究倫理審査申請書(変更) |
| 研究実施許可願の申請書 |
| 変更対比表 |
| 患者登録理由書(侵襲・介入のある研究は必須。※観察研究・疫学研究は不要) |
| 改訂を行った書類(研究者等リスト、研究計画書、説明同意書など、変更修正箇所がある書類) |
軽微な変更について
「研究計画書の軽微な変更に関する審査」に該当する事項のうち、下記に示す軽微な変更を行う場合は「軽微変更報告書」をご作成ください。事務局で報告事項に該当することを確認した上で、軽微変更報告書に確認日を記載します。その後、「軽微変更報告書」を交付することを以て当該変更を承認したとみなします。軽微変更報告書の記載方法の詳細は様式をご確認ください。
軽微な変更の提出書類
| 提出書類一覧 |
| 軽微変更報告書(臨床研究倫理委員会用) |
| 軽微変更報告書(疫学研究等倫理委員会用) |
| 改訂を行った書類(研究者等リスト、研究計画書、説明同意書など、変更修正箇所がある書類) |
軽微な変更に該当する事項
1.研究者の役職の変更
2.研究者の氏名の変更
3.鹿児島大学桜ヶ丘地区に所属する研究分担者の削除
4.jRCT(Japan Registry of Clinical Trials)の臨床研究実施計画番号の追記
5.症例登録期間の延長(研究実施予定期間が変わらない場合)
6.解析のための期間延長(症例登録が済んでいる場合)
7.目標症例数の変更(全体で変更がない場合)
8.倫理審査委員会の委員長交代に伴う変更
9.共同研究機関として参加する研究の個別審査であり本学の研究の実施に影響を与えない変更(例:他の共同研究機関の研究者の職名・氏名変更等)
軽微な変更の留意点
・軽微な変更に該当しない場合、通常の変更審査依頼に関する書類作成が必要です。
・軽微な変更の審査手続きは、迅速審査よりも手続きは簡便なものとなります。
・軽微な変更と通常の変更審査依頼が必要な変更内容が混在する場合、「軽微変更報告書」による変更の承認を得た後に、当該軽微な変更の内容を反映して別途、委員会審査を受けることも可能です。変更内容に応じて倫理審査委員会の事務局へご相談ください。
■初回審査時、臨床研究倫理委員会で審査した研究の提出先:臨床研究管理センター(crmc@m2.kufm.kagoshima-u.ac.jp)
申請書類一式は臨床研究管理センター宛てに電子メールで送信願います。
■初回審査時、疫学研究等倫理委員会で審査した研究の提出先:研究協力・倫理審査係(isgskkrs@kuas.kagoshima-u.ac.jp)
疫学研究等倫理委員会 | 鹿児島大学大学院 医歯学総合研究科 (kagoshima-u.ac.jp)
臨床研究倫理委員会・疫学研究等倫理委員会への中央一括審査の依頼
鹿児島大学桜ヶ丘地区臨床研究倫理委員会及び鹿児島大学桜ヶ丘地区疫学研究等倫理委員会では多機関共同研究について、原則、中央一括審査を行います。多機関共同研究を実施しようとする研究代表者は下記の事項に留意した上で一括した審査の申請に必要な書類を揃え、臨床研究管理センターへお申込みください。
多機関共同研究の研究計画書を申請しようとする研究代表者が留意すべき事項
原則、多機関共同研究の研究代表者は1つの倫理審査委員会による一括審査の手続きが必要です。🎯個別審査の要否について
一括審査が適切に実施された場合、他の機関において、改めて個別の倫理審査を行う必要はありません。🎯中央一括審査を申請する際の手続き
研究代表者が一の倫理審査委員会に審査を求める場合は、以下の手続きが必要です。
1⃣関係する共同研究機関と事前調整を行う。
↪各機関の📘研究者リスト・📘要件確認書の作成、COI・研究教育状況等を調整。
↪研究者の利益相反は、各機関の利益相反委員会で審査を受けるなどして管理願います。
2⃣審査依頼手続きを実施する。
3⃣各研究機関における研究実施体制に関する情報を提出する。
※研究実施体制(研究者、管理体制等)についても審査対象となります。
🎯計画書および説明文書・同意書の記載
✅多機関共同研究においては、全研究機関共通の研究計画書を作成してください。
✅説明文書および同意文書は、全研究機関共通の様式としてください。
💡作成上のポイント💡
🔹各研究機関の研究対象者に対する説明および同意に関する記載内容を一致させる。
🔹なお、研究機関ごとに異なる固有の事項は、編集可能な箇所として明示すること。
【編集可能な固有事項の例】
🔹相談窓口、問い合わせ先(電話番号・メールアドレス)
🔹補償窓口(該当する場合)
🔹個人情報管理責任者
🔹研究機関名、実施場所、研究責任者氏名・所属
🎯途中参加機関の取扱い
既に開始された研究に、新たに共同研究機関として参画する場合は、改めて変更審査が必要です。
↪このとき、同一の倫理審査委員会の意見を聴く必要があります。
🎯中央一括審査後の情報共有
中央一括審査を行った場合、研究代表者は、審査結果および承認資料を各共同研究機関へ共有してください。
【研究代表者が共有すべき資料】
📘審査結果通知書
📚IRB承認資料一式(研究計画書、情報公開文書、説明文書・同意書 等)
📌研究開始前の最重要事項📌
各機関の研究責任者は、これらの資料をもって、各機関の長から研究実施の許可を受けて下さい。
💡手続き上のポイント💡
中央一括審査の承認=研究開始可能、ではありません。必ず各機関の長の許可取得後に研究を開始すること。
臨床研究倫理委員会・疫学研究等倫理委員会で行う中央一括審査の流れ
| 下記の画像はこちらよりPDFダウンロード可能です。 |
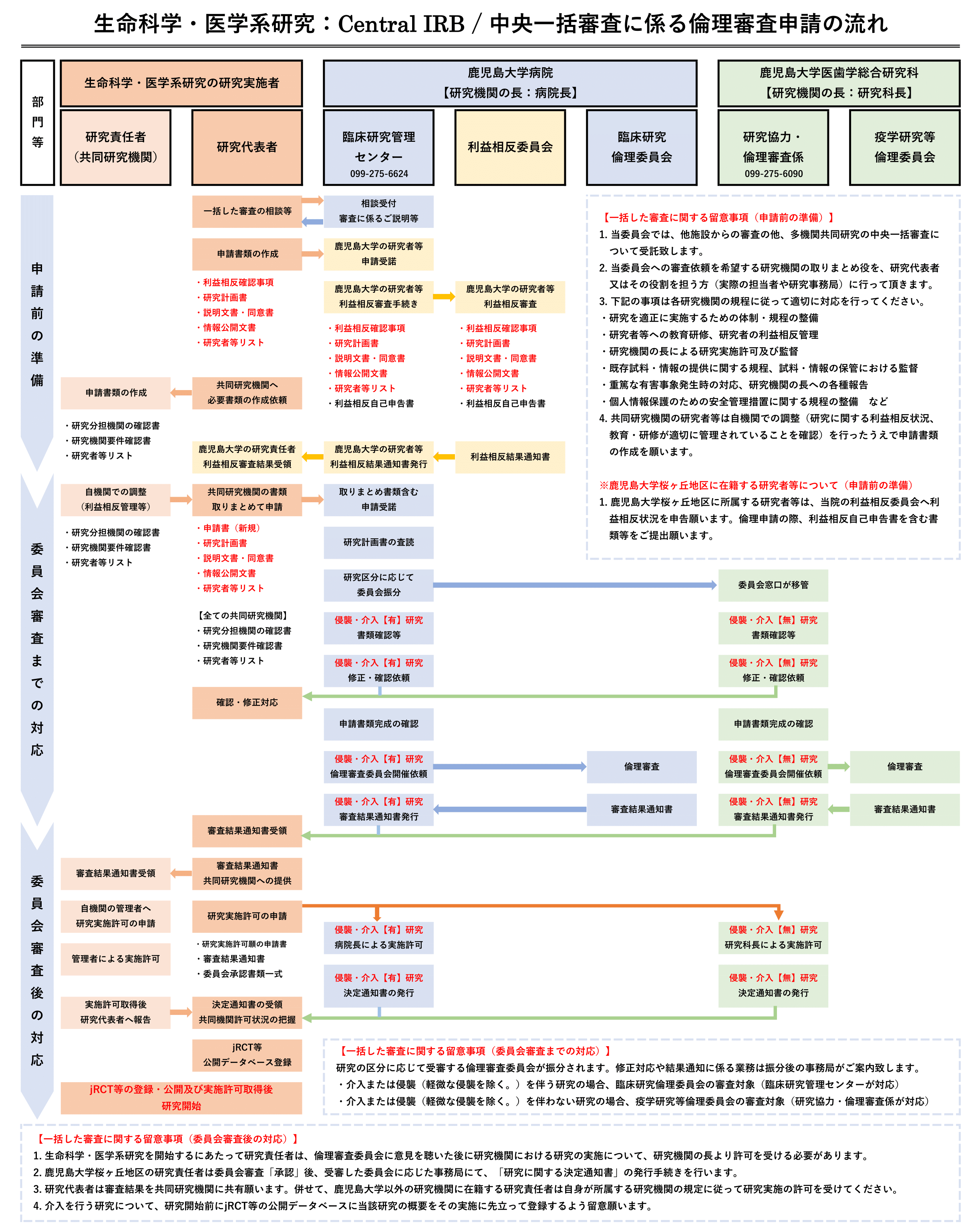
中央一括審査に関する書類提出先
中央一括審査に関する書類提出先は、通常の審査と同様となります。
新規審査依頼の場合、こちらをご覧下さい。変更審査依頼の場合、こちらをご覧下さい。
中央一括審査依頼の提出書類(新規審査依頼)
鹿児島大学桜ヶ丘地区の研究機関の長による研究実施許可
鹿児島大学桜ヶ丘地区に在籍する研究責任者は、倫理審査委員会に意見を聴いた後に、審査結果通知書及び倫理審査委員会に提出した書類、「研究実施許可願の申請書」を研究機関の長に提出し、当該研究機関における当該研究の実施について、許可を受けるようお願い致します。
生命科学・医学系研究の実施許可願の申請をしようとする研究責任者が留意すべき事項
🔹研究を開始する前に、研究機関の長による研究実施の許可を得てください。
🔹「変更」が生じた場合も、再度、委員会の承認と機関長の実施許可が必要です。
🔹倫理審査委員会が「不適当」と判断した研究は、実施できません。🎯不適合行為の防止と報告
🔸研究を行う際は、常に指針や法令に適合しているか確認して下さい。
🔸次の事実や懸念が判明した場合、速やかに研究機関の長に報告が必要です。
➤研究の実施の適正性や研究結果の信頼を損なう、または損なうおそれがある事実
➤研究対象者等の人権を侵害する懸念や、研究の実施上の重大な問題
➤研究に関連する情報の漏えい等の懸念🔸研究機関の長は、倫理審査委員会の意見を聴き、必要な対応を実施します。
↪以下の行為は重大な不適合とみなされます。
➤倫理審査委員会の審査や研究機関の長の許可を受けずに研究を実施した場合
➤必要なインフォームド・コンセントの手続を行わずに研究を実施した場合
➤研究内容の信頼性を損なう研究結果のねつ造や改ざんが発覚した場合
🔸この場合、研究の内容にかかわらず、大臣報告・公表が必要となる場合があります。
🎯研究者としての責務
◽許可前に研究を開始しない。
◽適正性・信頼性を確保するため、計画書・承認資料を常に最新の状態で管理。
◽共同研究の場合、研究代表者の指示や確認を受けつつ、自身の責任を果たす。
→つきましては、新規・変更審査の承認後は必ず「研究に関する決定通知書」の発行を受けて下さい。
| 様式 |
| 📘研究実施許可願の申請書(研究責任者→研究機関の長) |
| 📚IRB承認資料一式(審査結果通知書、計画書、情報公開文書など) |
研究実施許可願の申請に関する提出書類


「既存試料・情報の提供のみを行う者」の手続き
鹿児島大学桜ケ丘地区の部局が研究に主体的に関与(計画書の作成、論文執筆、解析・評価に関与)することなく、保有する既存試料・情報の提供のみを行う場合、倫理審査委員会の審査は不要とし、「他の研究機関への試料・情報の提供に関する(申請・報告)書」を予め提出のうえ、機関長の承認を得たうえで、既存試料・情報の提供を行うことが可能です。
まずは、下記の事項が研究計画書に記載されているかを確認して下さい。
🔁試料・情報の項目、取得の経緯、対応表の有無、保管期間等の必要事項が記載されているか?
🔁既存試料・情報の提供のみを行う者の所属機関に鹿児島大学が含まれているか?
※提供者が多数で個別特定が困難な場合は、計画書に提供者の属性を具体的に記載されているか?
「既存試料・情報の提供のみを行う者」として参画することが明確である場合、下記の書類を提出してください。その後、提供の可否に関する手続きが完了した後に、研究対象者へのオプトアウトなど、インフォームド・コンセントの手続きを正しく行った上で、既存試料・情報を提供してください。
既存試料・情報を提供する場合の提出書類
| 様式(提出先:臨床研究管理センター(crmc@m2.kufm.kagoshima-u.ac.jp)) |
| 📘他の研究機関への試料・情報の提供に関する(申請・報告)書 |
| 📚提供先のIRB承認資料一式(審査結果通知書、計画書、情報公開文書など) |
✅計画書作成前に保管・記録されていた試料やデータ(目的不問)
取得された目的は問わない。「研究計画書作成前」に対象者から取得済みであれば該当。
具体例
✔過去に診療で採取・保存されていた血液や組織
✔すでに記録されているカルテ情報
✔既存のデータベース情報✅計画書作成後に取得されたが別の目的(診療など)で収集されるもの
医療のため、別研究のため、健康調査・行政事業のためなど、その研究とは別目的で取得されたもの。
具体例
✔診療の過程で生じた残余検体、診療録情報
✔労働安全衛生規則に基づく健康調査データ
✔学校保健調査データ
✔地方公共団体の保健事業データ💡ポイント
🔹「既存試料・情報の提供のみを行う者」は「研究者等」には該当しない。
🔹計画書の作成、論文執筆、解析評価に関与する等、主体的に関与する場合は「研究者等」に該当する。
🎯試料・情報の提供に関する記録の作成・保管とは?
試料・情報の授受を行う場合、提供元&提供先では「試料・情報の提供に関する記録」の作成義務があります。
📒必要事項を記載した計画書を保管することは、記録義務の一部を満たす有効な手段です。
↪必要事項とは?:試料・情報の項目、取得経緯、対応表の有無、提供元のIC方法、保管期間等
📒他の研究機関への試料・情報の提供に関する申請・報告書は、手続き後も適切に保管してください。
📍提供元(既存試料・情報の提供のみを行う者)の保管期間:当該試料・情報の提供日から3年
📍提供先(研究者等)の保管期間:研究終了報告日から5年【研究責任者が記録を最終保管・管理】
「研究協力機関」の手続き
鹿児島大学桜ケ丘地区の部局が「研究協力機関」として研究対象者から新たに試料・情報を取得して研究機関に提供のみを行う場合、倫理審査委員会の審査は不要とし「他の研究機関への試料・情報の提供に関する(申請・報告)書」を予め提出のうえ、機関長に報告を行った上で、試料・情報の提供を行う必要があります。
まずは、下記の事項が研究計画書に記載されているかを確認して下さい。
🔁研究協力機関の所属機関一覧に鹿児島大学が含まれているか?
※「共同研究機関」や「既存試料・情報の提供のみを行う者」として参加するとあれば対象外です。
「研究協力機関」として参画することが明確である場合、下記の書類を提出してください。報告手続きが完了した後、外部機関の研究者等によるインフォームド・コンセントが正しく行われたことを確認してから、新たな試料や情報を収集・提供してください。
新たに試料・情報を取得して提供する場合の提出書類
| 様式(提出先:臨床研究管理センター(crmc@m2.kufm.kagoshima-u.ac.jp)) |
| 📘他の研究機関への試料・情報の提供に関する(申請・報告)書 |
| 📚提供先のIRB承認資料一式(審査結果通知書、計画書、情報公開文書など) |
研究に必要となる新たな試料・情報の収集のみを行い、研究機関へ提供のみを行う機関のことです。
具体例
✔学校、高齢者施設、役所や行政機関(アンケートや観察など非侵襲情報)
✔クリニック(採血や唾液採集など軽微な侵襲を伴う試料・情報収集)研究協力機関を介して新たに試料・情報を収集することが許容される範囲は?
✅侵襲を伴わない又は採血など、軽微な侵襲を伴う場合に限られます。
⭕侵襲なし(アンケート、行動観察、学習記録など)
⭕軽微な侵襲(採血、唾液採取など)
❌軽微を超える侵襲(外科的処置、身体的負担が大きい検査など)軽微を超える侵襲を伴う試料・情報は、研究協力機関のスタッフでは収集できません。
この場合、研究協力機関ではなく「共同研究機関」として参画させる必要があります。
IC(インフォームド・コンセント)の責任は誰にある?
✅研究実施の主体は「研究者等」であり、IC取得の責任は常に「研究者等」となります。
❌研究協力機関の施設スタッフや現場職員に説明と同意を任せることは、認められません。
💡補足:現場職員は協力・補助する立場で配布や回収、確認は手伝うことができます。
研究協力機関での報告・記録保管義務とは?
✅研究協力機関において試料・情報を収集する者は、研究協力機関の長に報告が必要です。
📒他の研究機関への試料・情報の提供に関する申請・報告書は、手続き後も適切に保管してください。
📍提供元(研究協力機関)の保管期間:当該試料・情報の提供日から3年
📍提供先(研究者等)の保管期間:研究終了報告日から5年【研究責任者が記録を最終保管・管理】
『外部』の倫理審査委員会を受審する生命科学・医学系研究の開始手続き
鹿児島大学桜ヶ丘地区の研究者が 外部の倫理審査委員会で審査を受ける場合、以下の手続きが必要です。
1.利益相反審査委員会への申告・審査・承認
📌当院の利益相反審査委員会(COI委員会)に対して、当該研究の利益相反の状態を申告します。
📌申告後、審査が承認となれば「利益相反反審査結果報告書」の発効を受けます。
📌審査に要する期間:1~2週間(〆切は設けず、随時受付)
📌外部の変更審査の際、鹿児島大学に影響しない変更内容であればCOI審査は不要です。
📌外部IRBのスケジュールを優先する場合は、IRB承認後の利益相反受審も可能です。
2.研究実施許可の取得
📌『外部』の倫理審査委員会で審査結果通知書(承認)発行後、全審査資料を添えて必ずご連絡をください。
📌承認資料から鹿児島大学が一括審査の対象であることが明記されていることを事前に確認して下さい。
📌後日、研究に関する決定通知書を発行します。これにより、研究の実施許可を正式に受けます。
📌生命科学・医学系研究の実施許可願の申請をしようとする研究責任者が留意すべき事項を参照下さい。
💡ポイント
🔹外部で審査を受けても、鹿児島大学内での利益相反の申告と許可取得は必須です。
🔹研究の実施許可は、外部審査の変更審査依頼が承認となった際にも必要となります。
💡研究実施機関の要件について
🔹『外部』の倫理審査委員会に審査依頼可能と規定した文書はこちらから参照可。
文書名:「人を対象とする生命科学・医学系研究標準業務手順書」(記載箇所:第8章6)
🔹利益相反に関する管理体制:あり(当院の利益相反審査委員会で審査)
🔹臨床研究に関する教育体制:あり(詳細はこちらから参照可)
『外部』の倫理審査委員会を受審する場合の手続きの流れについて
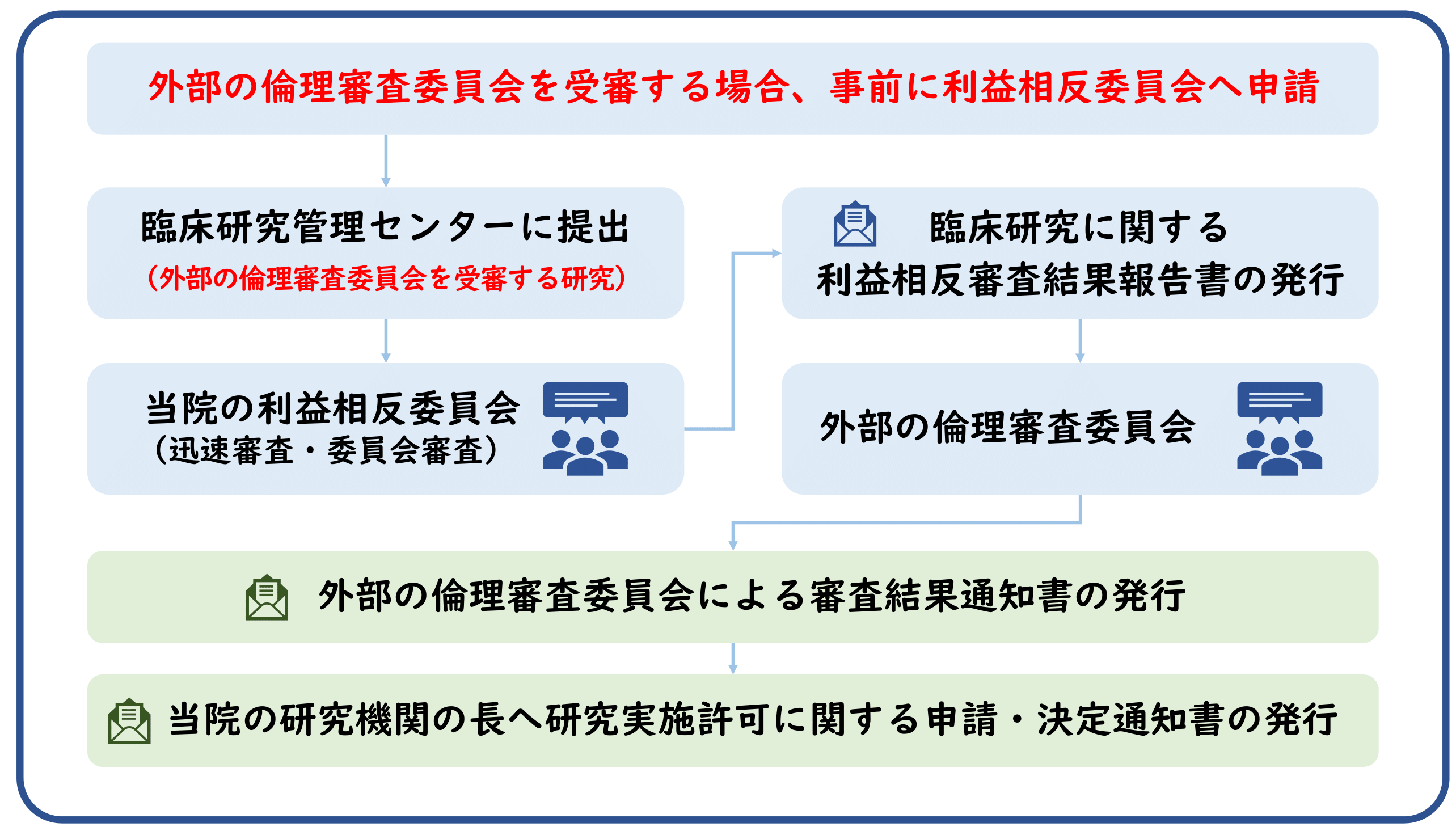
外部で審査を受けた研究の利益相反審査委員会への申告・審査のための提出書類
| 提出書類一覧 |
| 利益相反確認事項(生命科学・医学系研究倫理審査申請書(新規)p6の添付書類) |
| 研究実施許可願の申請書 |
| 利益相反自己申告書(概略) |
| 利益相反自己申告書(詳細)※ 利益相反自己申告書(概略)1.~4.の項目で「有」がある場合 |
| 研究者等リスト |
| 研究計画書 ※外部の倫理審査委員会を受審する際に提出する書類 |
| 説明文書・同意書 又は 情報公開文書 ※外部の倫理審査委員会を受審する際に提出する書類 |
| 外部の倫理審査委員会から発効された審査結果通知書(承認) |
| その他、IRBに提出し承認された全ての資料一式 |
外部の倫理審査委員会に意見を聴いた後の研究実施許可願の申請
外部の倫理審査委員会に意見を聴いた後に、審査結果通知書及び倫理審査委員会に提出した書類、「研究実施許可願の申請書」を研究機関の長に提出し、当該研究機関における当該研究の実施について、許可を受けるようお願い致します。研究機関の長による研究実施許可について、留意事項も含めてこちらをご覧下さい。
研究の概要の登録
研究責任者(多機関共同研究の場合は研究代表者)は、介入を行う研究について、厚生労働省が整備するデータベース(Japan Registry of Clinical Trials : jRCT) 等の公開データベースに、当該研究の概要をその実施に先立って登録し、研究計画書の変更及び研究の進捗に応じて更新する必要があります。また、それ以外の研究についても当該研究の概要をその研究の実施に先立って登録し、研究計画書の変更及び研究の進捗に応じて更新するよう努めなければなりません。
★データベース登録は、研究機関の長から実施の許可を受けた研究計画書に記載された研究期間が始まる前に行う必要がありますのでご留意願います。
| 公開データベース |
| 臨床研究実施計画・研究概要公開システム |
| UMIN臨床試験登録システム(UMIN-CTR) |
| 国立保健医療科学院のホームページ |
人を対象とする生命科学・医学系研究の研究期間について
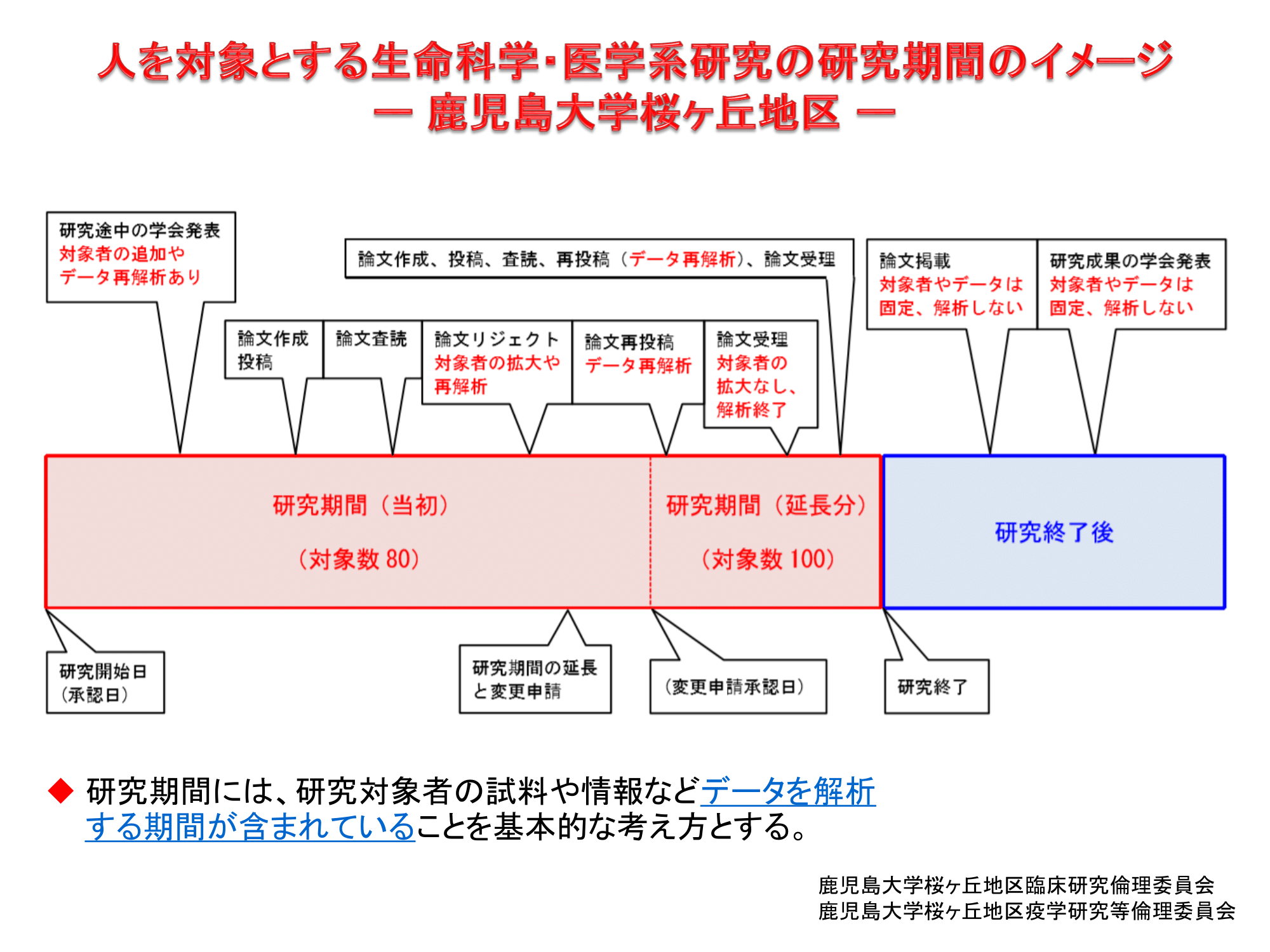
症例報告の倫理審査について
「人を対象とする生命科学・医学系研究に関する倫理指針」上は、症例発表時の倫理審査は必須ではございません。まずは発表する学会や雑誌等のルール・投稿規程等をご確認いただきますようお願い申し上げます。
ご案内(PDFダウンロード_学内のみ)
| 倫理審査申請書(症例報告用) |
各種様式について
書類作成前に、本ページ内(上にスクロール)の各項で必要書類をご確認ください。各項の「提出書類一式はこちら(ZIP)」より申請内容別にまとめてダウンロード可能です。まとめてダウンロードを希望しない場合に、下記より個別に様式をダウンロードすることが可能です。
| 利益相反(COI)審査申請に係る様式 |
| 利益相反自己申告書(概要) |
| 利益相反自己申告書(詳細) |
| 研究者等リスト |
| 生命科学・医学系研究の倫理審査申請に係る様式 |
| 生命科学・医学系研究倫理審査申請書(新規) |
| 生命科学・医学系研究倫理審査申請書(変更) |
| 生命科学・医学系研究実施計画書 |
| 説明文書・同意書・同意撤回通知書 |
| 情報公開文書 |
| 変更対比表 |
| 研究分担機関の確認書 |
| 研究機関要件確認書 |
| 倫理審査後、研究実施中~研究終了に係る様式 |
| 研究実施許可願の申請書 |
| 研究進捗状況報告書 |
| 研究(終了・中止・中断)報告書 |
| 重篤な有害事象に関する報告書(第1報) |
| 重篤な有害事象に関する報告書(第2報以降) |
| 生命科学・医学系研究に関する報告書(大学病院長宛て) |
| 生命科学・医学系研究に関する報告書(研究科長宛て) |
| その他様式 |
| 他の研究機関への試料・情報の提供に関する(申請・報告)書 |
| 臨床研究保険見積依頼書 |
| 倫理審査申請書(症例報告用) |
疫学研究等倫理委員会を利用して研究を実施中の研究者へ(未公開情報)
2026年度以降の倫理審査の体制変更について
これまで「侵襲(軽微な侵襲を除く)・介入を伴わない研究」で、疫学研究等倫理審査委員会(以下「疫学IRB」)に振り分けられて審査されていた研究(以下「疫学研究等」)については、2026年度より、鹿児島大学病院に設置される臨床研究倫理審査委員会(以下「病院IRB」)で審査を一本化する方針となりました。これにより、対象となる研究は順次、病院IRBでの審査へ移行が必要となります。
研究移管審査のご案内
今後「疫学研究等」を病院IRBで審査する際には、『研究移管』の手続きが必要となります。
研究者の皆様は、以下の資料をご確認のうえ手続きを進めてください。
📝研究移管手続きのフローチャート
📝改正指針に対応した新様式の運用
研究者の皆様にはご負担をおかけしますが、円滑な移行に向けてご協力をお願い申し上げます。
研究移管手続きのフローチャート
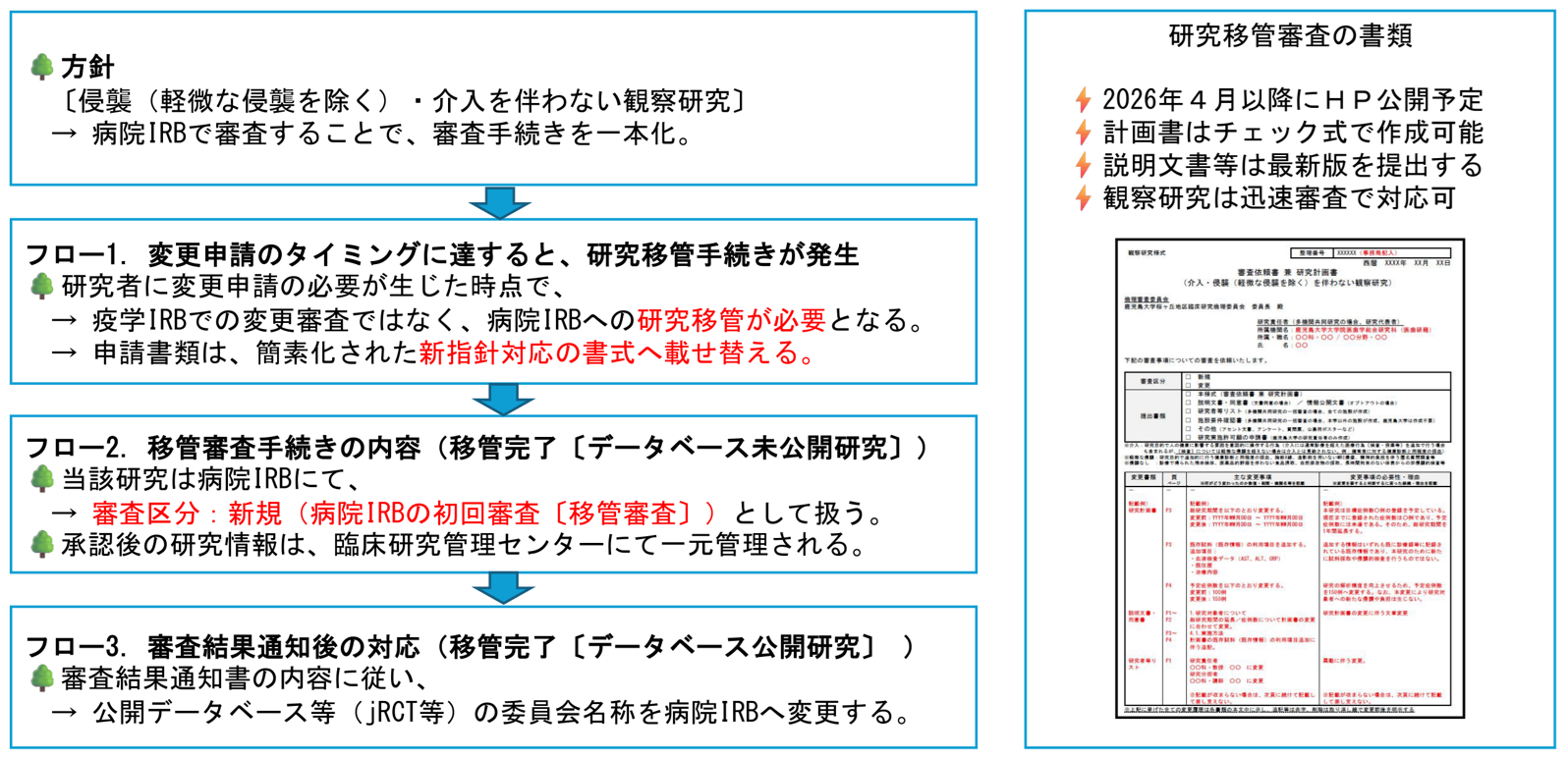
改正指針に対応した新様式の運用

新規審査依頼の書式一覧〔侵襲(軽微な侵襲を除く)・介入を伴わない研究〕
研究実施許可願の申請書WORD-
| 提出書類(※提出先:crmc@m2.kufm.kagoshima-u.ac.jp) | 書式 | 参考記載例 |
| 審査依頼書 兼 研究計画書 (侵襲(軽微な侵襲を除く)・介入を伴わない観察研究) |
WORD | - |
| 説明文書・同意書(観察研究様式) | WORD | - |
| 情報公開文書(観察研究様式) | WORD | - |
| 研究者等リスト(観察研究様式) | WORD | - |
| 研究機関要件確認書 | WORD | - |

 HOME
HOME 病院紹介
病院紹介 受診される方へ
受診される方へ 医療関係者の方へ
医療関係者の方へ 診療科案内
診療科案内 部門案内
部門案内 よくある質問
よくある質問 お問合せ
お問合せ アクセス・駐車場
アクセス・駐車場











